
| m |
| n |
| N |
| NA |
| m |
| n |
| 0.6mol |
| 2 |
| 19g |
| 0.2mol |
| 3.01×1023 |
| 6.02×1023mol-1 |
| 16g |
| 0.5mol |


科目:高中化学 来源: 题型:
| A、pH=0的溶液中:Na+、CH3COO-、Cl-、Cu2+ |
| B、pH=14的溶液中:H+、NH4+、SO42-、SO32- |
| C、使pH试纸变红的溶液中:Fe2+、CO32-、NO3-、Cl- |
| D、强酸性澄清透明溶液中:Al3+、K+、NO3-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、重金属离子对人体有剧毒,可采用沉淀反应除去之 |
| B、化肥中含有植物营养素,可大量使用以改善水环境 |
| C、轧钢厂排出的含盐酸的废水,可用熟石灰中和处理 |
| D、天然水中的细小悬浮颗粒,可用明矾等混凝剂净化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO+HNO3=N2O3+H2O |
| B、NH3+NO=HNO2+H2O |
| C、N2O4+H2O=HNO3+HNO2 |
| D、NO+CO=N2+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
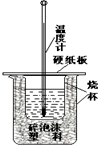 化学反应中一定伴随着能量的变化,化学能在实际生产生活中的应用将越来越广泛.
化学反应中一定伴随着能量的变化,化学能在实际生产生活中的应用将越来越广泛.| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主 食 | 米 饭 |
| 副 食 | 红烧鱼 |
| 饮 品 | 豆 浆 |
| 你的补充 | ? |
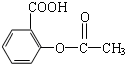 ,则其分子式为
,则其分子式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com