
| A. | 第一电离能:③>②>① | B. | 原子半径:③>②>① | ||
| C. | 电负性:③<②<① | D. | 最高正化合价:③>②>① |
分析 ①1s22s22p63s23p1基态原子的电子排布式是Al;②1s22s22p63s23p3基态原子的电子排布式是 P;③1s22s22p5基态原子的电子排布式是F,由此分析解答.
解答 解:A、非金属的第一电离能大于金属,而且非金属性越强,第一电离能越大,所以第一电离能:③>②>①,故A正确;
B、电子层数越多半径越大,电子层数相同时核电荷数越多半径越小,所以原子半径:①>②>③,故B错误;
C、非金属性越强电负性越大,所以电负性:③>②>①,故C错误;
D、氟的非金属性特强只显负价和和0价,没有正价,故D错误;
故选A.
点评 本题考查原子结构和元素周期律,为高频考点,侧重考查学生判断及元素周期律的灵活运用,正确判断元素、明确元素周期律内涵是解本题关键,注意第一电离能规律中的反常现象,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | △H=-2 878 kJ•mol-1 | B. | △H=-2 658 kJ•mol-1 | ||
| C. | △H=-1 746 kJ•mol-1 | D. | △H=-1 526 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烯 | B. | 一定有甲烷 | ||
| C. | 一定没有乙烯 | D. | 可能是甲烷和丁烯的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
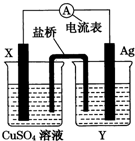 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②④⑤ | C. | ①②④ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 | |
| B. | 标准状况下,28 g CO和22.4 L H2O所含分子数相等 | |
| C. | 5.6 g铁粉与足量盐酸充分反应,有0.2 mol电子转移 | |
| D. | 等质量的CH4和NH3所含电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
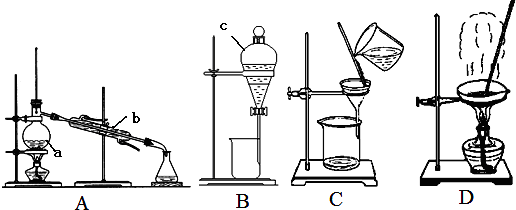
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
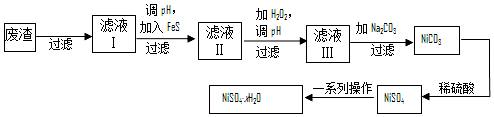
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com