

| A. | ④⑥ | B. | ①②③ | C. | ④⑤⑦ | D. | ①③④⑥ |
分析 ①电子层越多,半径越大;
②电子层越多,半径越大;
③根据图象判断;
④Na+带正电荷,Cl-带负电荷;
⑤氯化钠溶于水,形成水合离子;
⑥NaCl是强电解质,在溶液中完全电离;
⑦由图可知,钠离子和氯离子周围都存在水分子.
解答 解:①电子层越多,半径越大,Na+有2个电子层,Cl-有3个电子层,所以二者半径不同,故正确;
②电子层越多,半径越大,H原子只有1个电子层,O原子有2个电子层,所以氢和氧的半径不同,故正确;
③由图象可知,Na+周围有5个水分子,Cl-周围有6个水分子,所以Na+和Cl-周围的水分子数不同,故正确;
④Na+带正电荷吸引显负电性的O原子,Cl-带负电荷吸引显正电性的H原子,所以环绕在Na+和Cl-周围的水分子的排列方式不相同,故错误;
⑤氯化钠溶于水,形成水合离子,则物质的溶解是在水分子的作用下完成的,故正确;
⑥NaCl是强电解质,在溶液中完全电离,所以溶于水的NaCl完全电离,故错误;
⑦由图可知,钠离子和氯离子周围都存在水分子,即水溶液中的离子是以水合离子的形式存在的,故正确.
故选A.
点评 本题考查了电解质在溶液中的电离、微粒半径的比较等,题目难度不大,注意把握题目中图象中包含的信息,侧重于考查学生的分析能力和对信息的应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 炭和水反应吸收131.3kJ能量 | |
| B. | 1mol炭和1mol水反应生成CO和H2,并吸收131.3kJ热量 | |
| C. | 固态炭和水蒸气反应生成1mol CO气体和1mol H2气体,并吸热131.3kJ | |
| D. | 1个固态碳原子和1分子水蒸气反应吸热131.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | 苯甲酸 | 乙醇 | 环己烷 | 浓硫酸 | 苯甲酸乙酯 |
| 沸点/℃ | 249 | 78.3 | 80.7 | 338 | 212.6 |
 +CH3CH2OH$?_{60℃}^{浓H_{2}SO_{4}}$
+CH3CH2OH$?_{60℃}^{浓H_{2}SO_{4}}$ +H2O;实验装置中冷凝管的主要作用是冷凝回流.
+H2O;实验装置中冷凝管的主要作用是冷凝回流.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用PH试纸测定氯水的PH | |
| B. | 用硫酸镁溶液除去氢氧化镁中的氢氧化钙 | |
| C. | 用KSCN溶液检验Fe2+的存在 | |
| D. | 液溴保存时通常要加少量水液封 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
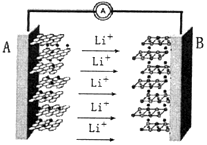 某手机电池采用了石墨烯电池,可充电5分钟,通话2小时.一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意图如图.已知参与电极反应的单位质量的电极材料放出电能的大小称为该电池的比能量.下列有关该电池说法不正确的是( )
某手机电池采用了石墨烯电池,可充电5分钟,通话2小时.一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意图如图.已知参与电极反应的单位质量的电极材料放出电能的大小称为该电池的比能量.下列有关该电池说法不正确的是( )| A. | 金属锂是所有金属中比能量最高的电极材料 | |
| B. | A电极为该电源的负极,发生氧化反应 | |
| C. | B电极的反应:2Li++S8+2e-═Li2S8 | |
| D. | 电子从A电极经过外电路流向B电极,再经过电解质流回A电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
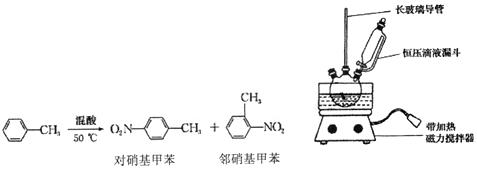
| 密度/(g•cm-3) | 沸点/℃ | 式量 | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 92 | 不溶于水,易溶于一硝基甲苯 |
| 对硝基甲苯 | 1.286 | 237.7 | 137 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 137 | 不溶于水,易溶于液态烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C可用于文物年代的鉴定,14C和12C互为同素异形体 | |
| B. | 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 | |
| C. | 高纯度的SiO2可以制成光电池将光能直接转化为电能 | |
| D. | 现代工业生产中芳香烃主要来源于石油化工的催化重整和煤的干馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
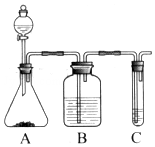 实验室常用如图中的装置制备乙炔并检验乙炔的性质:
实验室常用如图中的装置制备乙炔并检验乙炔的性质:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com