
【题目】下列物质不是配合物的是
A. K2[Co(NCS)4] B. Fe(SCN)3 C. CuSO45H2O D. NH4Cl
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分:
![]()
![]()
(1)①用酸性高锰酸钾溶液检验甲和乙中含有碳碳双键,方案是否可行 填“可行”或“不可行”)。
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 。
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物):

步骤Ⅰ的反应类型为 ,Y的结构简式 ,设计步骤Ⅰ的目的是 。
(3)1 mol乙最多可与 mol H2发生加成反应。
(4)写出乙与新制Cu(OH)2悬浊液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构的描述错误的是
A. 甲烷与氯气的混合气体在光照下生成的有机化合物均无同分异构体
B. 组成为C7H16的烷烃中仅能由一种单烯烃加氢而制得的有2种
C. 某烃的结构简式可表示为![]() (碳原子数≤10)。已知分子中有两种化学环境不同的氢原子,且数目之比为3∶2,则该烃一定是苯的同系物
(碳原子数≤10)。已知分子中有两种化学环境不同的氢原子,且数目之比为3∶2,则该烃一定是苯的同系物
D. 含5个碳原子的有机物,每个分子中最多可形成4个C—C键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小李在进行生物组织中化合物的鉴定时,向待测样液中滴加3滴苏丹Ⅲ染液。结果样液被染成橘黄色,说明样液中存在 ( )
A. 还原糖 B. 脂肪 C. 蛋白质 D. DNA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知一氧化碳与水蒸气的反应为: CO(g) + H2O(g)![]() CO2(g) + H2(g)
CO2(g) + H2(g)
在427 ℃ 时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0. 01 mol/L,则一氧化碳在此反应条件下的转化率为___________。
(2)规律是对经常出现的客观现象的归纳。规律越普遍,适用性或预言性也就越强,然而,任何规律都有其适用范围。
① 某同学在实验中发现,将H2S气体通入CuSO4溶液中,生成了黑色沉淀。请写出反应的化学方程式 ____________。
② 酸性强弱除与物质的本性有关外,还与溶剂有关,如CH3COOH与HF在液氨中可完全电离。在液氨中,反应CH3COONa + HCl = NaCl + CH3COOH _______(填“能”或“不能”)发生,理由是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
酸 | H2C2O4 | HF | H2CO3 | H2BO3 |
电离平衡常数Ka | Ka1=5.9×10-2 Ka2=6.4×10-5 | 未知 | Ka1=4.2×10-7 Ka2=5.6×10-11 | 5.8×10-10 |
(1)为了证明HF是弱酸,甲、乙、丙三位同学分别设计以下实验进行探究。
①甲同学取一定体积的HF溶液,滴入2滴紫色石蕊试液,显红色,再加入NaF固体观察到的现象是_______________,则证明HF为弱酸。
②乙同学取10ml未知浓度的HF溶液,测其pH为a,然后用蒸馏水稀释至1000ml。再测其pH为b,若要认为HF为弱酸,则a、b应满足的关系是b<_________(用含a的代数式表示)。
③丙同学用pH是指测得室温下0.10mol·L-1的HF溶液的pH为2,则测定HF为弱酸,由丙同学的实验数据可得室温下HF的电离平衡常数约为__________________。
(2)①已知H2BO3与NaOH溶液反应的离子方程式为H2BO3+OH-=B(OH)4,写出硼酸的电离方程式______________。
②向等浓度的H2C2O4与H2BO3混合溶液中逐滴加入NaOH溶液,则与OH-作用的粒子(包括分子和离子)依次为_____________,____________,____________。
③NaH C2O4溶液中加入少量的Na2CO3溶液,反应的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积均为500ml的I、II、III三个密闭容器中分别充入l molN2和2.5 molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下发生反应N2(g)+3H2(g) ![]() 2NH3(△H<0)。实验测得反应均进行到t min时N2的体积分数如图所示。下列说法正确的是
2NH3(△H<0)。实验测得反应均进行到t min时N2的体积分数如图所示。下列说法正确的是

A.当v(H2)=3v(N2)时,可以说明三个容器中的反应达平衡状态
B.在t min时,一定达化学平衡状态的是Ⅱ和Ⅲ
C.在t min时,测得c(N2)=1mol/L;若在向III中充入1.5molN2和1molNH3,H2的转化率不变
D.三个容器中的反应均达到平衡后,容器I中混合气体的平均相对分子质量最小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
组号 | 反应 | Na2S2O3 | H2SO4 | H2O | ||
体积/ mL | 浓度/ mol·L-1 | 体积/ mL | 浓度/ mol·L-1 | 体积/ mL | ||
A | 10 | 5 | 0.2 | 5 | 0.1 | 10 |
B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学通过查阅资料得到如下信息:草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,受热脱水、升华,易溶于水,170℃以上分解可得到CO、CO2、H2O,H2C2O4难溶于水。他们欲利用如下装置验证上述产物(加热仪器、夹持仪器省略)。
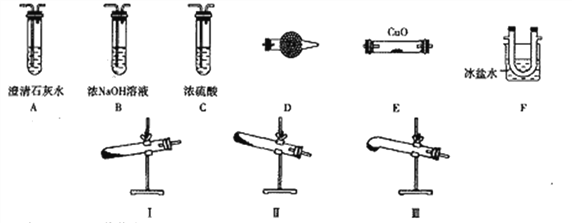
(1)加热草酸晶体使其分解的装置是________(从I、II、III中选取),验证其分解产物的装置依次是______→A→尾气处理装置(用装置字母作答,装置可重复使用)。
(2)D中试剂是_________,证明有CO生成的现象是_______。
(3)实验中有两处需要加热,加热的顺序是_________,写出一种处理尾气的方法:_____________。
(4)若上述实验均产生了预期的现象,写出草酸分解的化学方程式:_________________。
(5)设计一种方案证明草酸是弱酸_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com