
| A. | 元素的非金属性:X>W>Z | |
| B. | 元素W最高化合价和最低化合价的代数和为0 | |
| C. | Y与X能形成离子化合物 | |
| D. | 原子半径:Z>Y>X>W |
分析 原子序数依次增大的短周期元素W、X、Y、Z,它们的最外层电子数分别为4、6、1、4,则W、Z为IVA族元素,可推知W为C元素、Z为Si,Y的原子序数均大于碳,则Y为Na,X的原子序数小于Na,则X为O元素,据此解答.
解答 解:原子序数依次增大的短周期元素W、X、Y、Z,它们的最外层电子数分别为4、6、1、4,则W、Z为IVA族元素,可推知W为C元素、Z为Si,Y的原子序数均大于碳,则Y为Na,X的原子序数小于Na,则X为O元素.
A.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故元素的非金属性:X(O)>W(C)>Z(Si),故A正确;
B.W为C元素,最高正化合价为+4,最低负化合价为-4,二者之和为0,故B正确;
C.Y与X能形成氧化钠、过氧化钠,均属于离子化合物,故C正确;
D.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Y(Na)>Z(Si)>W(C)>X(O),故D错误,
故选:D.
点评 本题考查结构位置性质关系应用,元素的推断是解答本题的关系,注意对元素周期律的理解掌握,题目难度不大.


科目:高中化学 来源: 题型:解答题
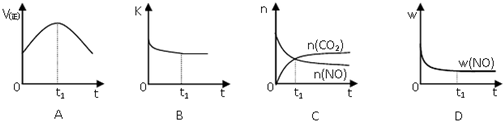
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| C. | NaHCO3溶液与稀H2SO4反应:CO${\;}_{3}^{2-}$+2H+═H2O+CO2↑ | |
| D. | NaOH溶液与NaHSO4溶液反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
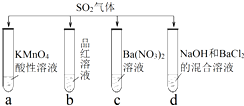
| A. | 试管a中实验可以证明具有漂白性 | |
| B. | 试管b中溶液褪色,说明具有强氧化性 | |
| C. | 试管c中能产生白色沉淀,说明具有还原性 | |
| D. | 试管d中能产生白色沉淀,该沉淀完全溶于 稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要配制浓度为0.25mol•L-1的NaOH溶液480mL,应称量4.8g NaOH在250mL的烧杯中溶解,冷却,再转移到500mL容量瓶中,洗涤、转移、定容 | |
| B. | 配制NaOH溶液,在烧杯中溶解NaOH后未冷却至室温就转移到容量瓶中,溶液浓度偏低 | |
| C. | 配制一定物质的量浓度的溶液定容时,俯视刻度线导致所配浓度偏高 | |
| D. | 配制20g密度为ρg•cm-3的Ca(NO3)2溶液中含有2g Ca(NO3)2,则溶液中NO3-的物质的量浓度为25ρ/41mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
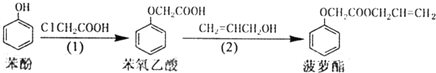
| A. | 步骤(1)、(2)的反应类型不同 | |
| B. | 步骤(1)产物中残留的苯酚能用FeCl3溶液检验 | |
| C. | 苯氧乙酸和菠萝酯均可与氢氧化钠溶液反应 | |
| D. | 步骤(2)产物中残留的烯丙醇不能用溴水检验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com