
分析 (1)漂白粉的主要成分为氯化钙和Ca(ClO)2,次氯酸根离子具有强氧化性;
(2)发现溶液先变蓝色后褪色,说明溶液呈碱性,且具有强氧化性;
(3)氯气通入石灰乳,反应生成氯化钙和次氯酸钙;
(4)漂白粉露置在空气中变质,是次氯酸钙可与二氧化碳发生反应生成碳酸钙和次氯酸;
(5)NaClO3中氯氯元素化合价+5价变化为+4价,HCl中氯元素化合价-1价变化为0价,电子转移2e-;
解答 解:(1)漂白粉的主要成分为氯化钙和Ca(ClO)2,次氯酸根离子具有强氧化性,则Ca(ClO)2为有效成分,故答案为:Ca(ClO)2;
(2)发现溶液先变蓝色后褪色,说明溶液呈碱性,原因是次氯酸钙为强碱弱酸盐,水解呈碱性,水解生成的HClO具有强氧化性,具有漂白作用,故答案为:BC;
(3)氯气通入石灰乳,反应生成氯化钙和次氯酸钙,反应的方程式为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(4)漂白粉露置在空气中变质,是次氯酸钙可与二氧化碳发生反应生成碳酸钙和次氯酸,反应的化学方程式为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
(5)反应中HCl为还原剂,被氧化生成氯气,化合价由-1价升高到0价,NaClO3中氯氯元素化合价+5价变化为+4价做氧化剂,电子转移2e-,
用双线桥法标出电子转移的方向和数目为: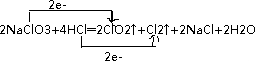
答:用双线桥法标出电子转移的方向和数目为: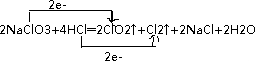 ;
;
点评 本题考查漂白粉的性质及制备,注意利用信息提供的反应物与生成物书写反应,侧重化学反应方程式及氧化还原反应的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
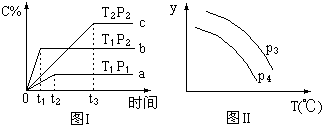 在某容积一定的密闭容器中,有下列的可逆反应:(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
在某容积一定的密闭容器中,有下列的可逆反应:(g)+B(g)?xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )| A. | P3>P4,y轴表示A的物质的量 | |
| B. | P3<P4,y轴表示B的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钙溶液和氢氧化钠溶液混合 HCO3-+OH-═CO32-+H2O | |
| B. | 醋酸钠溶液和盐酸混合 CH3COONa+H+═CH3COOH+Na+ | |
| C. | 少量金属钠放入冷水中 Na+2H2O═Na++2OH-+H2↑ | |
| D. | 硫酸铜溶液和氢氧化钡溶液混合 Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:3 | C. | 2:3 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲法多 | B. | 乙法多 | C. | 一样多 | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
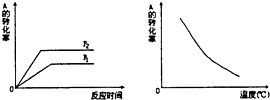 如图所示,可逆反应:mA(g)+nB(g)?xC(g),在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是( )
如图所示,可逆反应:mA(g)+nB(g)?xC(g),在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是( )| A. | 放热,m+n>x | B. | 放热,m+n<x | C. | 吸热,m+n<x | D. | 吸热,m+n>x |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将置于海水中的钢铁设备作为阴极,接上直流电源和辅助阳极,使其受到保护的方法叫牺牲阳极的阴极保护法 | |
| B. | 200mlmol/LFe2(SO4)3溶液,Fe3+和SO42-,离子总数为NA | |
| C. | 10g 46%的乙醇水溶液中所含氢原子数目为1.2NA | |
| D. | 可用电解氯化镁溶液的方法制取金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
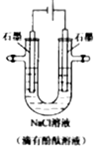 用石墨作电极,电解盛放在U形管中的饱和溶液和NaCl溶液(滴有酚酞溶液),如图,下列叙述正确的是( )
用石墨作电极,电解盛放在U形管中的饱和溶液和NaCl溶液(滴有酚酞溶液),如图,下列叙述正确的是( )| A. | 通电后,NaCl发生电离 | |
| B. | 通电一段时间后,阳极附近溶液先变红 | |
| C. | 当阳极生成0.1mol气体时,整个电路中转移了0.1mole- | |
| D. | 电解饱和食盐水的总反应式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com