
分析 (1)①对于吸热反应,升高温度平衡向正反应方向移动;
②2CH4(g)═C2H4(g)+2H2(g)可看作是①×2-②-③得到的,根据盖斯定律来计算反应的焓变;
(2)据平衡常数可计算得平衡时各物质的浓度,再根据转化率=$\frac{转化浓度}{起始浓度}$×100%计算.
解答 解:(1)①该反应为吸热反应,升高温度平衡向正反应方向移动,所以平衡常数增大,故答案为:增大;
②由①CH4(g)+2O2(g)═CO2(g)+2H2O ( l )△H=-890.3kJ•mol-1
②C2H4(g)+3O2(g)═2CO2(g)+2H2O ( l )△H=-1 306.4kJ•mol-1
③2H2(g)+O2(g)═2H2O ( l )△H=-571.6 kJ•mol-1
则2CH4(g)═C2H4(g)+2H2(g)可看作是①×2-②-③得到的,
所以根据盖斯定律,反应的△H=-890.3kJ•mol-1×2+1 306.4kJ•mol-1+571.6 kJ•mol-1=+97.4 kJ•mol-1,
故答案为:+97.4 kJ•mol-1;
(2)设甲烷转化的浓度为xmol/L
CH4(g)+H2O(g)?CO(g)+3H2(g)
起始(mol/L) 2 2 0 0
转化(mol/L) x x x 3x
平衡(mol/L) 2-x 2-x 3x
根据K=$\frac{x×(3x)^{3}}{(2-x)×(2-x)}$=27,解得x=1,所以CH4的平衡转化率=$\frac{1}{2}$×100%=50%,
故答案为:50%.
点评 本题考查平衡计算与移动、平衡常数的计算以及盖斯定律的应用等知识,难度中等,注意盖斯定律和平衡移动原理的灵活运用是关键.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:解答题
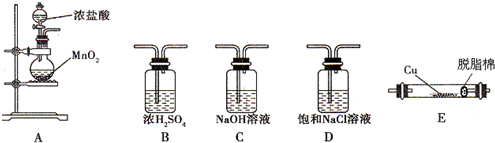
 ;若在标准状态下收集到2.24L氯气,则被氧化的HCl的物质的量是0.2mol.
;若在标准状态下收集到2.24L氯气,则被氧化的HCl的物质的量是0.2mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知一定温度和压强下,在起始容积为V L的容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+B(g)?C(g)△H>0.达到平衡时,C的体积分数为40%.试回答:
已知一定温度和压强下,在起始容积为V L的容器中充入1mol A和1mol B,保持恒温恒压下反应:A(g)+B(g)?C(g)△H>0.达到平衡时,C的体积分数为40%.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和NaOH反应的中和热△H=-57.3kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | CO(g)的燃烧热是283.0 kJ•mol-1,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0 kJ•mol-1 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g);△H12C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/ (mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用甲除去CO气体中的CO2气体 | |
| B. | 用乙分离沸点相差较大的互溶液体混合物 | |
| C. | 丙向容量瓶中转移液体 | |
| D. | 用丁分离互不相溶的两种液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苏打-NaHCO3 | B. | 酒精-C2H5OH | C. | 明矾-KAl (SO4)2 | D. | 烧碱-Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com