
| A£® | v£ØC£©=0.5mol/£ØL•min£© | |
| B£® | x=3 | |
| C£® | BµÄ×Ŗ»ÆĀŹĪŖ25% | |
| D£® | ČōŹ¹ÓĆ“ß»Æ¼ĮæÉŅŌĖõ¶Ģ“ļµ½Ę½ŗāµÄŹ±¼ä£¬µ«A×Ŗ»ÆĀŹ²»±ä |
·ÖĪö 2sŗóAµÄ×Ŗ»ÆĀŹĪŖ50%£¬æÉÖŖ×Ŗ»ÆµÄAĪŖ2mol”Į50%=1mol£¬ÓÉ·“Ó¦æÉÖŖÉś³ÉCĪŖ1mol£¬v£ØC£©=$\frac{\frac{1mol}{2L}}{2s}$=0.25mol•L-1•s-1£¬v£ØD£©=0.25mol•L-1•s-1£¬ÓÉĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±ČæÉÖŖ£¬x=2£¬Ōņ
2A£Øg£©+3B£Øg£©?2C£Øg£©+2D£Øg£©£¬
æŖŹ¼ 2 2 0 0
×Ŗ»Æ 1 1.5 1 1
2s 1 0.5 1 1
ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ2sŗóAµÄ×Ŗ»ÆĀŹĪŖ50%£¬æÉÖŖ×Ŗ»ÆµÄAĪŖ2mol”Į50%=1mol£¬ÓÉ·“Ó¦æÉÖŖÉś³ÉCĪŖ1mol£¬v£ØC£©=$\frac{\frac{1mol}{2L}}{2s}$=0.25mol•L-1•s-1£¬v£ØD£©=0.25mol•L-1•s-1£¬ÓÉĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±ČæÉÖŖ£¬x=2£¬Ōņ
2A£Øg£©+3B£Øg£©?2C£Øg£©+2D£Øg£©£¬
æŖŹ¼ 2 2 0 0
×Ŗ»Æ 1 1.5 1 1
2s 1 0.5 1 1
A£®ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬v£ØC£©=0.25mol•L-1•s-1£¬¹ŹA“ķĪó£»
B£®ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬z=2£¬¹ŹB“ķĪó£»
C£®BµÄ×Ŗ»ÆĀŹĪŖ$\frac{1.5}{2}$”Į100%=75%£¬¹ŹC“ķĪó£»
D£®“߻ƼĮ½µµĶ·“Ó¦µÄ»ī»ÆÄÜ£¬Ķ¬µČ³Ģ¶Čøı䷓ӦĖŁĀŹ£¬Ę½ŗā²»ŅĘ¶Æ£¬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ»ÆŃ§Ę½ŗāČż¶Ī·Ø”¢×Ŗ»ÆĀŹµÄ¼ĘĖćµČĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓė¼ĘĖćÄÜĮ¦µÄ漲飬עŅā·“Ó¦ÖŠĪļÖŹµÄĮæµÄ¹ŲĻµ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŠ£ĆūŹ¦ÅąÓÅ×÷Ņµ±¾¼ÓŗĖŠÄŹŌ¾ķĻµĮŠ“š°ø
ĆūŠ£ĆūŹ¦ÅąÓÅ×÷Ņµ±¾¼ÓŗĖŠÄŹŌ¾ķĻµĮŠ“š°ø Č«³Ģ½š¾ķĻµĮŠ“š°ø
Č«³Ģ½š¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄÅØĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®
ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄÅØĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.08 | B£® | 0.04 | C£® | 0.032 | D£® | 0.036 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
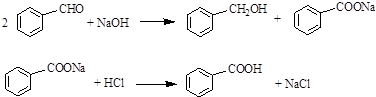
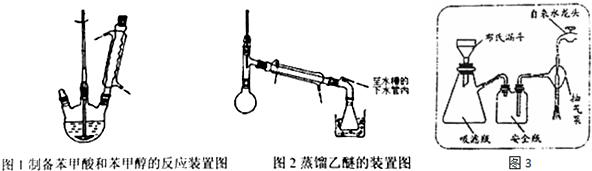
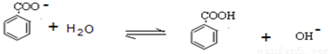 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| H2CO3 | H2SO3 | HNO2 | HClO |
| K1=4.4”Į10-7 K2=4.7”Į10-11 | K1=1.2”Į10-2 K2=6.6”Į10-8 | K=7.2”Į10-4 | K=2.9”Į10-8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
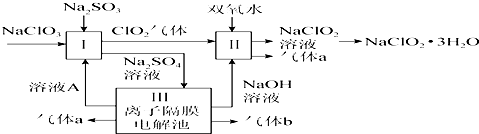
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
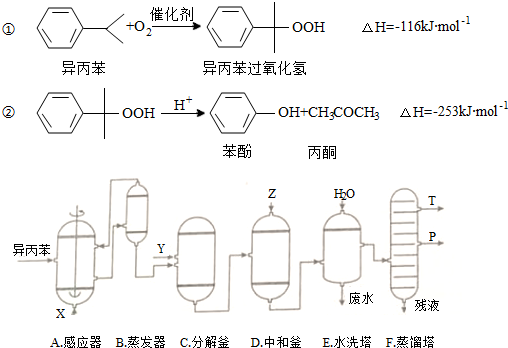
| ĪļÖŹ | Ļą¶Ō·Ö×ÓÖŹĮæ | ĆÜ¶Č£Øg/cm-3£© | ·Šµć/”ę |
| Ņģ±ū±½ | 120 | 0.8640 | 153 |
| ±ūĶŖ | 58 | 0.7898 | 56.5 |
| ±½·Ó | 94 | 1.0722 | 182 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ³É ·Ö | NaCl | Mg£ØOH£©2 | CaCO3 | BaSO4 | ĘäĖū²»ČÜÓŚĖįµÄĪļÖŹ |
| ÖŹĮæ·ÖŹż/% | 15”«20 | 15”«20 | 5”«10 | 30”«40 | 10”«15 |
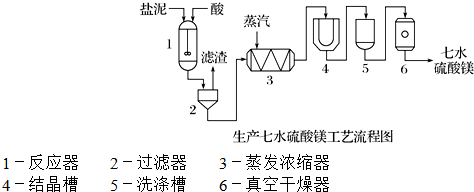
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com