

| 261 |
| x |
| 233 |
| mg |
| 261m |
| 233 |
| 261m | ||
|
| 261m |
| 233w |
| 261m |
| 233w |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、常温常压下,46gNO2和N2O4的混合物含有的氮原子数为NA |
| B、标准状况下,22.4L NH3溶于足量水中产生的NH4+数目为NA |
| C、标准状况下,22.4L SO3所含的分子数为NA |
| D、通常状况下,56 g Fe与任何物质完全反应时转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它的元素符号为O |
| B、它的核外电子排布式为1s22s22p63s23p4 |
| C、可以与H2化合生成液态化合物 |
D、其原子轨道式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
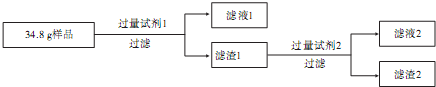
| 试剂1 | 试剂2 | 滤渣1质量 | 滤渣2质量 | |
| 实验一 | 稀盐酸 | NaOH溶液 | 12.4g | 6.4g |
| 实验二 | NaOH溶液 | 稀盐酸 | 28.8g | 6.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 编 号 | 猜 想 |
| 甲 | 溶液中的Fe3+又被还原为Fe2+ |
| 乙 | 溶液中的SCN-被过量的氯水氧化 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
| 编号 | 实验操作 | 预期现象和结论 |
| ① | | |
| | | |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、用图1所示装置除去中含有的少量Cl2 |
| B、用图2所示装置蒸发AlCl3溶液制备无水AlCl3 |
| C、用图3所示装置可以完成“喷泉”实验 |
| D、硝图4所示装置制取并收集干燥纯净的NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com