
| A.碳酸钙分解 |
| B.酸碱中和 |
| C.焦碳在高温下与水蒸气反应 |
| D.Ba(OH)2?8H2O与NH4Cl(固体)的反应 |
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.CaO+H2O=Ca(OH)2 | ||||
B.2Na+O2
| ||||
C.Fe2O3+2Al
| ||||
D.右图所示的反应为吸热反应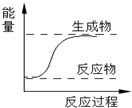 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1  CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1 C(s)+CO2(g) ΔH=-171kJ·mol-1
C(s)+CO2(g) ΔH=-171kJ·mol-1 CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
 CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CuSO4(s)+5H2O(1),热效应为ΔH3。则下列判断正确的是( )
CuSO4(s)+5H2O(1),热效应为ΔH3。则下列判断正确的是( )| A.ΔH2>ΔH3 | B.ΔH1<ΔH3 | C.ΔH1+ΔH3=ΔH2 | D.ΔH1+ΔH2=ΔH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g) +H2(g) ΔH=" +131.3" kJ?mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2的产率的是 。(填序号)
CO(g) +H2(g) ΔH=" +131.3" kJ?mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2的产率的是 。(填序号)| A.升高温度 | B.增加碳的用量 | C.加入催化剂 | D.用CO吸收剂除去CO |
 2CO(g) △H=+172.5kJ?mol-1
2CO(g) △H=+172.5kJ?mol-1 CO2(g)+H2(g)的△H=
CO2(g)+H2(g)的△H=  CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:| t / min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。| 离子 | H+ | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol·L-1 | 未测定 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
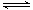 2NO(g) △H
2NO(g) △H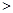 0
0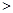 0,判断该设想能否实现并简述其依据: 。
0,判断该设想能否实现并简述其依据: 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com