
| A. | K2SO4、HNO3、BaCl2 | B. | NaOH、NH4Cl、Mg(NO3)2 | ||
| C. | NH4HCO3、KCl、NaCl | D. | KMnO4、NaCl、H2SO4 |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则物质大量共存,并结合离子的颜色来解答.
解答 解:A.K2SO4、BaCl2反应生成硫酸钡沉淀,不能大量共存,故A错误;
B.NaOH、NH4Cl反应生成一水合氨,NaOH、Mg(NO3)2反应生成氢氧化镁沉淀,不能大量共存,故B错误;
C.该组物质自己不反应,可大量共存,且溶于水均为无色,故C正确;
D.KMnO4、NaCl、H2SO4发生氧化还原反应生成氯气,且KMnO4为紫色,与无色不符,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
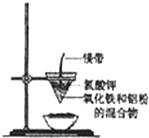 研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
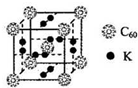
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2 HCl | B. | ClO2 NaClO2 | C. | NaCl HClO | D. | KClO3 Ca(ClO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
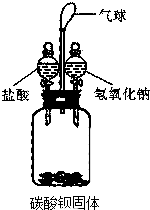 某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)
某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
| 除去干扰物 | ①取广口瓶中溶液少量于试管中,向其中加入过量CaCl2溶液,充分反应后过滤 | 有白色沉淀 产生 | 溶质中还含有NaOH |
| 检验是否 含有NaOH | 在滤液中滴加酚酞试液 | 溶液变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
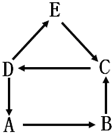 A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题:
A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.9 mol | B. | 0.8 mol | C. | 0.7 mol | D. | 0.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | NaCl NaBr | C. | NaCl NaBr NaI | D. | NaCl NaI |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com