
A、亚硫酸氢铵溶液与含等物质的量的NaOH的溶液混合:N
| |||||||||||||||
B、氢氧化钡溶液与硫酸氢钠溶液反应至溶液恰好呈中性:Ba2++2H++SO42-+2OH-
| |||||||||||||||
C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-
| |||||||||||||||
D、向碳酸氢镁溶液中加入过量澄清石灰水:Mg2++2HC
|


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| CaSO4 | 9.0×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E各物质的转化关系如图所示.
A、B、C、D、E各物质的转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MnS的Ksp比CuS的Ksp大 | ||
| B、该反应达到平衡时c(Mn2+)=c(Cu2+) | ||
| C、往平衡体系中加入少量CuSO4固体后,C(Mn2+)变大 | ||
D、该反应的平衡常数K=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②③④ |
| C、①③④ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.请回答下列问题:
已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、247.3 kJ |
| B、494.6 kJ |
| C、2.76×103kJ |
| D、5.52×103kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
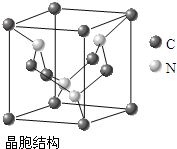 [化学-物质结构与性质]
[化学-物质结构与性质]| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com