
| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 元素周期表第ⅠA族元素都是金属元素 | |
| C. | Cl-、S2-、Ca2+、K+半径逐渐减小 | |
| D. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力相同 |
分析 A.同主族元素最高价含氧酸自上而下酸性减弱;
B.第ⅠA族元素氢是非金属元素;
C.电子层结构相同,核电数越多半径越小;
D、最外层电子数相同所以得电子能力相同.
解答 解:A.同主族元素最高价含氧酸自上而下酸性减弱,不是最高价含氧酸不一定,如HClO为弱酸、HBrO4为强酸,故A错误;
B.第ⅠA族元素氢是非金属元素,故B错误;
C.电子层结构相同,核电数越多半径越小,所以半径大小为:S2->Cl->K+>Ca2+,故C错误;
D、${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl质子数相同,所以最外层电子数相同,得电子能力相同,故D正确;
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素周期律、周期表中的族序数、原子序数等关系为解答的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释 | |
| B. | 用热的纯碱(Na2CO3)溶液容易洗去餐具上的油污 | |
| C. | 向牛奶中加入果汁会产生沉淀,这是因为酸碱发生了中和反应 | |
| D. | 用铁制自来水管与铜制水龙头连接使用时,连接处的铁水管锈蚀更快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P、S、N | B. | Cl、S、F | C. | S、Cl、O | D. | K、Ca、Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H278Se的稳定性比H2S稳定性强 | |
| B. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同素异形体 | |
| C. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se组成的气态物质属于化合物 | |
| D. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同位素,分别含有44和46个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
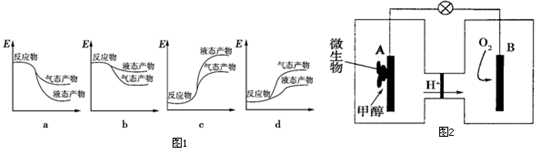
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极反应为H2+2OH--2e-═2H2O | |
| B. | 放电时负极有CO2生成 | |
| C. | 该电池供应2 mol水蒸气,同时转移2 mol电子 | |
| D. | 该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CH2 | B. | CH2=CHCH=CH2 | C. | CH3=CHCH3 | D. | CH3-C≡CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑩ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com