
| A. | m=4 R2+是还原剂 | B. | m=n R3+是氧化产物 | ||
| C. | m=2 R2+是氧化剂 | D. | m=y R3+是还原产物 |
分析 xR2++yH++O2═mR3++nH2O中,由原子守恒可知,x=m,n=2,y=4,由电荷守恒可知,2x+4=3m,所以m=4,该反应中R元素的化合价升高,O元素的化合价降低,以此来解答.
解答 解:xR2++yH++O2═mR3++nH2O中,由原子守恒可知,x=m,n=2,y=4,由电荷守恒可知,2x+4=3m,所以m=4,该反应中R元素的化合价升高,O元素的化合价降低,
A.m=4,R2+是还原剂,R3+是氧化产物,故A正确;
B.m=4,n=2,R3+是氧化产物,故B错误;
C.m=4,R2+是还原剂,故C错误;
D.m=y,R3+是氧化产物,故D错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意电子、电荷守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铁与稀硫酸反应Fe+2H+═Fe3++H2↑ | |
| B. | 氢氧化铝与足量盐酸反应Al(OH)3+3H+═Al3++3H2O | |
| C. | 钠和冷水反应 Na+2H2O═Na++H2↑+OH- | |
| D. | 金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4溶液中滴加入Ba(OH)2溶液至中性H++Ba2++OH-+SO42-═BaSO4↓+H2O | |
| B. | 酸性KMnO4溶液与双氧水反应:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 钢铁腐蚀时可能发生的正极反应为:4OH-+4e-═2H2O+O2↑ | |
| D. | 将氯气溶于水制备次氯酸:Cl2+H2O?2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将等体积、等物质的量浓度的CH3COONH4与CH3COONa溶液混合:c(CH3COO-)>c(Na+)>c(NH4+)>c(OH-) | |
| B. | 将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体后的溶液:c(H+)+c(H2CO3)=c(OH-)+c(CO32-)+c(NH3•H2O) | |
| C. | 向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-) | |
| D. | 向0.10mol•L-1 Na2CO3溶液中通入少量CO2的溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 固体质量 | 加入某浓度盐酸的体积/mL | 加入某浓度NaOH的体积/mL | 收集到气体体积/mL |
| 1 | 0.9 | 20.0 | ─ | 1008 |
| 2 | 0.9 | 30.0 | ─ | 1008 |
| 3 | 0.9 | ─ | 20.0 | 672 |
| 4 | 0.9 | ─ | 30.0 | 672 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 标准状况下气体的体积(mL) | 280 | 336 | 336 |
| A. | 甲、乙组的实验中,盐酸均是过量的 | B. | 盐酸的物质的量浓度为0.8mol L-1 | ||
| C. | 合金中镁、铝的物质的量之比为1:1 | D. | 丙组中铝的物质的量为0.0045mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
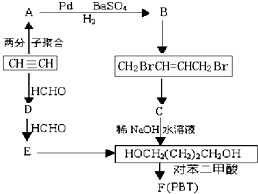 请根据以下知识解答
请根据以下知识解答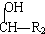 (R代表烃基,下同.)
(R代表烃基,下同.)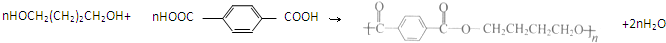 .
.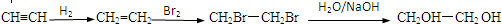 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,1mol N2与足量H2混合反应生成NH3,转移电子数6NA | |
| B. | 在常温常压下,2.8g N2和CO的混合气体所含电子数为1.4NA | |
| C. | 标准状况下,22.4L CCl4含有的分子数目为NA | |
| D. | 在电解精炼粗铜的过程中,当转移电子数为NA时,阳极溶解32g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com