

分析 (1)①仪器A是分液漏斗;
②装置B中制取氯气,利用二氧化锰与浓盐酸发生反应生成氯化锰、氯气、水,写出化学方程式再改写成离子方程式;
③实验中的反应物之一为氯气,若过量会污染大气,所以需要处理尾气;
④从CuCl2溶液中得到晶体,应通过加热浓缩,冷却结晶,再过滤、干燥;
(2)因Cu2+能水解且加热会促进水解生成Cu(OH)2,同时得到挥发性的酸盐酸,根据平衡理论,要通过加入稀盐酸抑制水解平衡正向移动,提高产品纯度.
解答 解:(1)①仪器A是分液漏斗,故答案为:分液漏斗;
②装置B中制取氯气,二氧化锰与浓盐酸发生反应的化学方程工为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,改写后得到离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
③实验中的反应物之一为氯气,应考虑到过量的氯气能污染大气,所以需要处理尾气,一般用NaOH溶液吸收,故答案为:NaOH溶液;吸收多余的氯气,防止空气污染;
④从溶液里得到固体溶质,通常采用的分离方法是结晶法,具体过程是蒸发浓缩、冷却结晶、过滤、干燥,故答案为:蒸发浓缩、冷却结晶;
(2)由CuCl2溶液得到CuCl2•2H2O的过程中Cu2+水解,要加盐酸防止Cu2+水解,否则产品中会含有Cu(OH)2杂质,故答案为:抑制Cu2+水解,提高产品产率(或纯度).
点评 本题考查学生对工艺流程理解、实验装置的理解、盐类水解的应用,物质分离提纯等,中等难度.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤⑦ | B. | ②④⑤⑥⑦ | C. | ①④⑤⑥⑦ | D. | ②③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 开始沉淀的pH | 沉淀完全的pH | |
| Al3+ | 3.2 | 4.4 |
| Fe2+ | 6.3 | 8.4 |
| Ca2+ | 11.8 | \ |
| Mg2+ | 8.8 | 10.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 催化剂组分质量分数(%) | CuO | 0 | 25 | 50 | 75 | 100 |
| ZnO | 100 | 75 | 50 | 25 | 0 | |
| 到达平衡所需时间(h) | 2.5 | 7.4 | 8.1 | 12 | 无催化活性 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
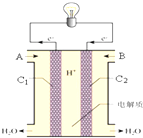 氢氧燃料电池已用于航天飞机.如图为氢氧燃料电池构造示意图,其中A、B为气体进口,C1、C2均为石墨电极,电解质溶液为30%的氢氧化钾溶液.
氢氧燃料电池已用于航天飞机.如图为氢氧燃料电池构造示意图,其中A、B为气体进口,C1、C2均为石墨电极,电解质溶液为30%的氢氧化钾溶液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com