
在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①增大反应物的浓度 ②升高温度 ③增大压强 ④移去生成物 ⑤加入催化剂
A.①③⑤B.②⑤C.②③⑤D.①③④
科目:高中化学 来源:2014年高二化学苏教版选修2 2.1氨的合成练习卷(解析版) 题型:选择题
在NH3、HNO3、H2SO4的工业生产中,具有的共同点是( )。
A.使用吸收塔设备 B.使用加压条件
C.使用氢气做原料 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 9化学平衡常数练习卷(解析版) 题型:填空题
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是( )
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 7化学平衡状态的建立及标志练习卷(解析版) 题型:选择题
一定条件下,发生如下反应:2A(g)+2B(g)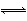 3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
A.单位时间内生成n mol B,同时消耗3n mol C
B.容器内压强不随时间而变化
C.混合气体的密度不随时间变化
D.单位时间内生成2n mol A,同时生成n mol D
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 7化学平衡状态的建立及标志练习卷(解析版) 题型:选择题
在一定温度下,将等物质的量的CO和水蒸气通入恒容密闭容器中,发生如下反应:
CO(g)+H2O(g) CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是( )
CO2(g)+H2(g),一段时间后反应达到平衡。对该平衡状态描述正确的是( )
A.正反应速率等于零
B.正反应速率大于逆反应速率
C.正反应速率等于逆反应速率
D.正反应速率小于逆反应速率
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 6影响化学反应速率的因素练习卷(解析版) 题型:选择题
反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量
B.将容器的体积缩小一半
C.保持体积不变,充入H2O(g)使体系压强增大
D.保持压强不变,充入N2使容器体积变大
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 5化学反应速率练习卷(解析版) 题型:选择题
在容积为2 L的密闭容器中充入2 mol SO2和一定量O2,发生反应2SO2+O2 2SO3,当反应进行到4 min时,测得n(SO2)=0.4 mol。若反应进行到2 min末时,容器中SO2的物质的量是( )
2SO3,当反应进行到4 min时,测得n(SO2)=0.4 mol。若反应进行到2 min末时,容器中SO2的物质的量是( )
A.等于1.6 molB.等于1.2 molC.大于1.6 molD.小于1.2 mol
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 4化学反应热的计算练习卷(解析版) 题型:选择题
下列关于反应热的说法正确的是( )
A.当ΔH为“-”时,表示该反应为吸热反应
B.已知C(s)+O2(g) CO(g)的反应热为-110.5 kJ·mol-1,说明碳的燃烧热为110.5 kJ·mol-1
CO(g)的反应热为-110.5 kJ·mol-1,说明碳的燃烧热为110.5 kJ·mol-1
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
查看答案和解析>>
科目:高中化学 来源:2014年高二化学人教版选修四 20燃料电池练习卷(解析版) 题型:选择题
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )
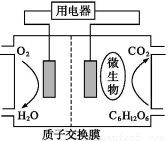
A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e- 6CO2↑+24H+
6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com