
����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���____________________________��
A��C(s)+H2O(g)=CO(g)+H2(g) ��H>0
B��2H2(g)+O2(g)=2H2O(1) ��H<0
C��NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) ��H<0
����KOH��ҺΪ�������Һ��������ѡ��Ӧ���һ��ԭ��أ��������ĵ缫��ӦʽΪ_______________��
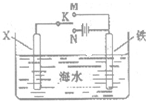
�ǵ��ԭ���ڻ�ѧ��ҵ�����Ź㷺��Ӧ�á��ֽ�����Ƶ�ԭ���ͨ����������ͼ�е�������������aΪ���Һ��X��Y��Ϊ���Ե缫����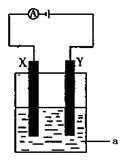
����aΪCuSO4��Һ������ʱ�Ļ�ѧ��Ӧ����ʽΪ____________________________________��
������⺬��0.04molCuSO4��0.04molNaCl�Ļ����Һ400ml������������������672 mL����״���£�ʱ����Һ��pH = �����������Һ������䣩��
��1��B
��2��O2 + 4eһ + 2 H2O = 4OHһ
��3����
��1
���������������1��������Ŀ����������Ϣ������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ���ų�A������Ϊ�����ԭ��صķ�Ӧ������������ԭ��Ӧ������ѡ��Bѡ���2���ڼ�����Һ��������ӦΪ��O2 + 4eһ + 2 H2O = 4OHһ����3���ٵ������ͭ��Һ�����Ļ�ѧ��Ӧ����ʽΪ��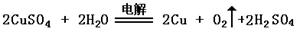 �ڵ��CuSO4��Һ��NaCl�����Һ�����ķ�ӦΪ��Cu2++2e- =Cu,������ӦΪ��2Cl--2e-=Cl2����������һ����672 mL��Ϊ0.03mol�����ȫ����������������������Ҫ0.06mol��������Ŀ���Ȼ���Ϊ0.04mol���������Ӳ��㣬����ṩ0.04mol�����ӣ������������0.02mol��������ʣ�µ�0.01mol����������������������������ӷŵ�������������ӷŵ硣Ҫ����0.01mol���������ݵ缫��Ӧʽ������Ҫ0.04mol�����������ӣ�������Һ����ˮ�������������Ҳ��0.04mol��Ũ��Ϊ0.1mol/L��PH=1��
�ڵ��CuSO4��Һ��NaCl�����Һ�����ķ�ӦΪ��Cu2++2e- =Cu,������ӦΪ��2Cl--2e-=Cl2����������һ����672 mL��Ϊ0.03mol�����ȫ����������������������Ҫ0.06mol��������Ŀ���Ȼ���Ϊ0.04mol���������Ӳ��㣬����ṩ0.04mol�����ӣ������������0.02mol��������ʣ�µ�0.01mol����������������������������ӷŵ�������������ӷŵ硣Ҫ����0.01mol���������ݵ缫��Ӧʽ������Ҫ0.04mol�����������ӣ�������Һ����ˮ�������������Ҳ��0.04mol��Ũ��Ϊ0.1mol/L��PH=1��
���㣺���أ�ԭ��صĹ�������
����������ϸ�µؿ����˵�����ԭ��أ�ÿһ��С�����漰�Ķ��ǵ�����ԭ��صij����ص�֪ʶ��ѧ����Ҫ�������գ������һ��С��PH�ļ����У��ؼ���Ҫ��������ŵ�˳���ܽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com