
”¾ĢāÄæ”æ·°£Ø23V)ŹĒĪŅ¹śµÄ·į²śŌŖĖŲ£¬¹ć·ŗÓĆÓŚ“߻Ƽ°øÖĢś¹¤Ņµ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©·°ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ_______£¬Ęä¼Ū²ćµē×ÓÅŲ¼Ķ¼ĪŖ____________”£
£Ø2£©·°µÄijÖÖŃõ»ÆĪļµÄ¾§°ū½į¹¹ČēĶ¼1ĖłŹ¾”£¾§°ūÖŠŹµ¼ŹÓµÓŠµÄŅõ”¢ŃōĄė×ÓøöŹż·Ö±šĪŖ____”¢_____”£
£Ø3£©V2O5³£ÓĆ×÷SO2×Ŗ»ÆĪŖSO3µÄ“߻ƼĮ”£SO2·Ö×ÓÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌŹżŹĒ__¶Ō£¬·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖ___£»SO3ĘųĢ¬ĪŖµ„·Ö×Ó£¬øĆ·Ö×ÓÖŠSŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ____£»SO3µÄČż¾ŪĢ廷ד½į¹¹ČēĶ¼2ĖłŹ¾£¬øĆ½į¹¹ÖŠSŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ___£»øĆ½į¹¹ÖŠS”ŖO¼ü³¤ÓŠĮ½Ąą£¬Ņ»Ąą¼ü³¤Ō¼140pm£¬ĮķŅ»Ąą¼ü³¤Ō¼ĪŖ160pm£¬½Ļ¶ĢµÄ¼üĪŖ__£ØĢīĶ¼2ÖŠ×ÖÄø)£¬øĆ·Ö×ÓÖŠŗ¬ÓŠ___øö¦Ņ¼ü”£

£Ø4£©V2O5ČܽāŌŚNaOHČÜŅŗÖŠ£¬æɵƵ½·°ĖįÄĘ£ØNa3VO4)£¬øĆŃĪŅõĄė×ÓµÄĮ¢Ģå¹¹ŠĶĪŖ___£»Ņ²æÉŅŌµĆµ½Ę«·°ĖįÄĘ£¬ĘäŅõĄė×Ó³ŹČēĶ¼3ĖłŹ¾µÄĪŽĻŽĮ“ד½į¹¹£¬ŌņĘ«·°ĖįÄʵĻÆѧŹ½ĪŖ_______”£
”¾“š°ø”æ µŚ4ÖÜĘŚ¢õB×å ![]() 4 2 3 VŠĪ sp2ŌÓ»Æ sp3ŌÓ»Æ a 12 ÕżĖÄĆęĢåŠĪ NaVO3
4 2 3 VŠĪ sp2ŌÓ»Æ sp3ŌÓ»Æ a 12 ÕżĖÄĆęĢåŠĪ NaVO3
”¾½āĪö”æŹŌĢā·ÖĪö£ŗ£Ø1£©ÓÉĢāŅāÖŖ£¬·°µÄŗĖµēŗÉŹżĪŖ23£¬ŌņæÉŅŌĶĘÖŖ·°ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖµŚ4ÖÜĘŚ¢õA×壬øł¾ŻŗĖĶāµē×ӵĹģµĄÄÜĮæÅŲ¼Ė³Šņ£¬æÉŅŌĶʶĻĘäµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d34s2£¬“¦ÓŚdĒų£¬·°“¦ÓŚµŚĖÄÖÜĘŚµŚ¢õB×壬Ęä¼Ū²ćµē×ÓÅŲ¼Ķ¼ĪŖ![]() ”£
ӣ
£Ø2£©Óɾ§°ūæÉÖŖ£¬VĪ»ÓŚ¶„µćŗĶĢåŠÄ£¬ŃōĄė×ÓøöŹżĪŖ1+8”Į1/8=2£¬OÓŠ4øöĪ»ÓŚĆęŠÄ£¬2øöĪ»ÓŚĢåŠÄ£¬ŌņŅõĄė×ÓøöŹżĪŖ4”Į1/2+2=4£¬ĖłŅŌ¾§°ūÖŠŹµ¼ŹÓµÓŠµÄŅõ”¢ŃōĄė×ÓøöŹż·Ö±šĪŖ4,2.
£Ø3£©SO2·Ö×ÓÖŠSŌ×ÓŠĪ³É2øö¼ü£¬¹Āµē×Ó¶ŌŹżĪŖ£Ø6-2”Į2£©”Ā2=1£¬SO2·Ö×ÓÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌŹżŹĒ3£¬ĪŖVŠĪ½į¹¹£¬SO3ĘųĢ¬ĪŖµ„·Ö×Ó£¬øĆ·Ö×ÓÖŠSŌ×ÓŠĪ³É3øö¼ü£¬Ć»ÓŠ¹Ā¶Ōµē×Ó£¬ŌņĪŖsp2Ōӻƣ¬SO3µÄČż¾ŪĢåÖŠSŌ×ÓŠĪ³É4øö¼ü£¬ĪŖsp3Ōӻƣ»SO3µÄČż¾ŪĢåÖŠĆæøöS“ęŌŚS=O¼üŗĶS-O¼ü£¬S=O¼ü³¤½Ļ¶Ģ£¬¼“a½Ļ¶Ģ£¬øĆ·Ö×ÓÖŠŗ¬ÓŠ¼üŹżÄæĪŖ3”Į4=12
£Ø4£©VO43-ÖŠ£¬VŠĪ³É4øö¼ü£¬¹Āµē×Ó¶ŌŹżĪŖ£Ø5+3-4”Į2£©”Ā2=0£¬ĪŖÕżĖÄĆęĢå½į¹¹£¬ÓÉĮ“ד½į¹¹æÉÖŖĆæøöVÓė3øöOŠĪ³ÉŅõĄė×Ó£¬ĒŅVµÄ»ÆŗĻ¼ŪĪŖ+5¼Ū£¬ŌņŠĪ³ÉµÄ»ÆŗĻĪļ»ÆѧŹ½ĪŖNaVO3”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĪļÖŹÖŠ£¬µŚŅ»ÖÖŹĒĖį£¬µŚ¶žÖÖŹĒ»ģŗĻĪļ£¬µŚČżÖÖŹĒ¼īµÄŹĒ
A. æÕĘų”¢ĮņĖįĶ”¢ĮņĖįB. “×Ėį”¢ŅŗĀČ”¢“æ¼ī
C. ĻõĖį”¢Ź³ŃĪĖ®”¢ÉÕ¼īD. Ńõ»ÆĢś”¢µØ·Æ”¢ŹģŹÆ»Ņ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹żŃõ»ÆÄĘŹĒŅ»ÖÖµ»ĘÉ«¹ĢĢ壬ĖüÄÜÓė¶žŃõ»ÆĢ¼·“Ӧɜ³ÉŃõĘų£¬ŌŚĒ±Ė®Ķ§ÖŠÓĆ×÷ÖĘŃõ¼Į£¬¹©Ķ§Ō±ŗōĪüÖ®ÓĆ£¬ĖüÓė¶žŃõ»ÆĢ¼·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2Na2O2£«2CO2=2Na2CO3£«O2”£Ä³Ń§ÉśĪŖĮĖŃéÖ¤ÕāŅ»ŹµŃ飬ŅŌ×ćĮæµÄ“óĄķŹÆ”¢×ćĮæµÄŃĪĖįŗĶ1.95g¹żŃõ»ÆÄĘѳʷĪŖŌĮĻ£¬ÖĘČ”O2£¬Éč¼Ę³öČēĻĀŹµŃé×°ÖĆ£ŗ
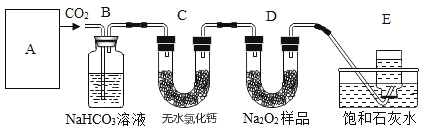
£Ø1£©AÖŠÖĘČ”CO2µÄ×°ÖĆ£¬Ó¦ĪŖĻĀĮŠĶ¼¢Ł”¢¢Ś”¢¢ŪÖŠµÄĶ¼____________£»
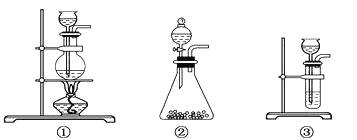
B×°ÖƵÄ×÷ÓĆŹĒ________£¬ĪŖĮĖ¼ģŃéEÖŠŹÕ¼Æµ½µÄĘųĢ壬ŌŚČ”³ö¼ÆĘųĘæŗó£¬_____________£»
£Ø2£©ČōEÖŠµÄŹÆ»ŅĖ®³öĻÖĒįĪ¢°×É«»ė×Ē£¬ĒėĖµĆ÷ŌŅņ£ŗ_________________£»
£Ø3£©·“Ó¦Ķź±ĻŹ±£¬Čō²āµĆEÖŠµÄ¼ÆĘųĘæŹÕ¼Æµ½µÄĘųĢåĪŖ250 mL£¬ÓÖÖŖŃõĘųµÄĆܶČĪŖ1£®43 g/L£¬µ±×°ÖƵÄĘųĆÜŠŌĮ¼ŗƵÄĒéæöĻĀ£¬Źµ¼ŹŹÕ¼Æµ½µÄŃõĘųĢå»ż±ČĄķĀŪ¼ĘĖćÖµ________(Ģī”°“ó”±»ņ”°Š””±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ: 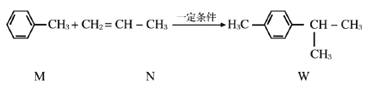 ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. M”¢NŗĶW¾łÄÜ·¢ÉśŃõ»Æ·“Ó¦”¢¼Ó³É·“Ó¦ŗĶČ”“ś·“Ó¦
B. M²»ÄÜŹ¹äåĖ®Ņņ·¢Éś»Æѧ·“Ó¦¶ųĶŹÉ«
C. MÓė×ćĮæµÄH2·“Ó¦ŗóµÄ²śĪļµÄŅ»ĀČ“śĪļÓŠ4ÖÖ
D. WµÄĖłÓŠĢ¼Ō×Ó²»æÉÄÜŌŚĶ¬Ņ»Ę½ĆęÉĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē½āÖŹČÜŅŗµēµ¼ĀŹŌ½“óµ¼µēÄÜĮ¦Ō½Ē攣³£ĪĀĻĀÓĆ0.100mol/LŃĪĖį·Ö±šµĪ¶Ø10.00mLÅØ¶Č¾łĪŖ0.100mol/LµÄNaOHČÜŅŗŗĶ¶ž¼×°·[(CH3)2NH]ČÜŅŗ(¶ž¼×°·ŌŚĖ®ÖŠµēĄėÓė°±ĻąĖĘ£¬³£ĪĀĻĀKb=1.6”Į10-4)”£ĄūÓĆ“«øŠĘ÷²āµĆµĪ¶Ø¹ż³ĢÖŠČÜŅŗµÄµēµ¼ĀŹČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
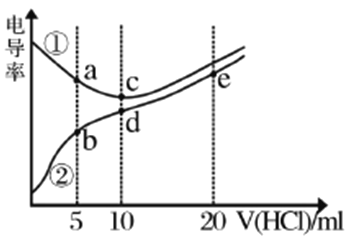
A. a”¢d”¢eČżµćµÄČÜŅŗÖŠ£¬Ė®µÄµēĄė³Ģ¶Č×ī“óµÄŹĒdµć
B. ČÜŅŗĪĀ¶ČcµćøßÓŚdµć
C. bµćČÜŅŗÖŠ:c[(CH3)2NH2+]+c[(CH3)2NH”¤H2O]=2c(Cl-)
D. dµćČÜŅŗÖŠ:c(H+)+ c[(CH3)2NH”¤H2O]=c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)Rµ„ÖŹµÄ¾§ĢåŌŚ²»Ķ¬ĪĀ¶ČĻĀÓŠĮ½ÖÖŌ×Ӷѻż·½Ź½£¬¾§°ū·Ö±šČēĻĀĶ¼ĖłŹ¾”£AÖŠŌ×Ӷѻż·½Ź½ĪŖ________¶Ń»ż£¬A”¢BÖŠRŌ×ÓµÄÅäĪ»ŹżÖ®±ČĪŖ________”£
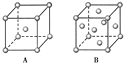
(2)ŅŃÖŖµ„ÖŹDĪŖĆęŠÄĮ¢·½¾§Ģ壬ČēĶ¼ĖłŹ¾£¬DµÄĻą¶ŌŌ×ÓÖŹĮæĪŖM£¬ĆܶČĪŖ8.9 g/cm3”£

ŹŌĒó£ŗ
¢ŁĶ¼ÖŠÕż·½ŠĪ±ß³¤£½________cm(Ö»ĮŠ³ö¼ĘĖćŹ½£¬NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ)”£
¢ŚŹŌ¼ĘĖ浄֏D¾§ĢåÖŠŌ×ÓµÄæÕ¼äĄūÓĆĀŹ£ŗ________(ĮŠ³ö¼ĘĖćŹ½²¢»Æ¼ņ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĆ¾-æÕĘųµē³ŲµÄ¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬µē³Ų·“Ó¦·½³ĢŹ½ĪŖ:2Mg+O2+2H2O=2Mg(OH)2”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
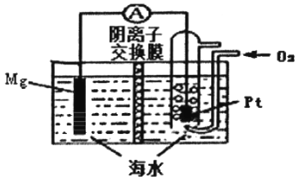
A. ĶØČėŃõĘųµÄµē¼«ĪŖÕż¼«
B. ·ÅµēŹ±£¬ČÜŅŗÖŠµÄOH-ÓÉÕż¼«ŅĘĻņøŗ¼«
C. øŗ¼«µÄµē¼«·“Ó¦ĪŖMg-2e-=Mg2+
D. ²ÉÓƶąæ×Ptµē¼«ÓŠĄūÓŚŃõĘųĄ©É¢£¬Ģįøßµē¼«Óėµē½āÖŹČÜŅŗµÄ½Ó“„¶ų»ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ±ź×¼×“æöĻĀ£¬Ņ»Ńõ»ÆĢ¼ŗĶ¶žŃõ»ÆĢ¼µÄ»ģŗĻĘųĢå5.6L£¬Čē¹ū¶žŃõ»ÆĢ¼µÄÖŹĮæĪŖ2.2g£¬ŌņŅ»Ńõ»ÆĢ¼µÄÖŹĮæĪŖ£Ø £©
A. 5.6g B. 4.4g C. 2.8g D. 1g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬A”¢B”¢CČżøöČŻĘ÷ÖŠ¾ł½ųŠŠĶ¬Ņ»øö·“Ó¦£ŗN2(g)+3H2(g) ![]() 2NH3(g) ¦¤H =£ Q kJ”¤mol£1£¬ŌŚĻąĶ¬µÄŹ±¼ä¶ĪÄŚ£¬²āµĆČēĻĀŹż¾Ż£ŗ
2NH3(g) ¦¤H =£ Q kJ”¤mol£1£¬ŌŚĻąĶ¬µÄŹ±¼ä¶ĪÄŚ£¬²āµĆČēĻĀŹż¾Ż£ŗ
ČŻĘ÷ | A | B | C |
·“Ó¦ĖŁĀŹ/mol”¤L-1”¤min-1 | v(H2) = 3 | v(N2) = 3 | v(NH3) = 4 |
ŌņČżøöČŻĘ÷·Å³öµÄČČĮæQµÄ“󊔹ŲĻµĪŖ£Ø £©
A. B > C > A B. A > B > C C. C > A > B D. B > A > C
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com