
 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/10-10m | 0.66 | 1.36 | 1.23 | 1.10 | 0.99 | 1.54 | 0.70 | 1.18 |
| 最高化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| A、元素④⑤形成的化合物是离子化合物 |
| B、元素⑦的气态氢化物稳定性比元素④的气态氢化物稳定性强 |
| C、元素①⑧形成的化合物具有两性 |
| D、上表8种元素中,元素③的最高价氧化物对应水化物的碱性最强 |


科目:高中化学 来源: 题型:
(2010?清远模拟)下表为短周期元素①~⑧的部分性质,下列说法正确的是( )
|
查看答案和解析>>
科目:高中化学 来源:2014届江西省高一第一次段考化学试卷 题型:选择题
已知下表为短周期元素①~⑧的部分性质。
|
|
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10m |
0.73 |
1.30 |
1.34 |
1.06 |
0.99 |
1.54 |
0.75 |
1.18 |
|
最高化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
最低化合价 |
-2 |
|
|
-3 |
-1 |
|
-3 |
|
下列说法正确的是( )
A.元素④⑤形成的化合物是离子化合物
B.元素⑦的气态氢化物稳定性比元素④的气态氢化物稳定性弱
C.元素①⑧形成的化合物具有两性
D.上表8种元素中,元素③的最高价氧化物对应水化物的碱性最强
查看答案和解析>>
科目:高中化学 来源:2012届高二年级高考复习方案配套课标版(二)月考化学试卷 题型:选择题
下表为短周期元素①~⑧的部分性质。
|
元素编号 元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10m |
0.66 |
1.36 |
1.23 |
1.10 |
0.99 |
1.54 |
0.70 |
1.18 |
|
最高化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
最低化合价 |
—2 |
|
|
—3 |
—1 |
|
—3 |
|
下列说法正确的是 A.元素④⑤形成的化合物是离子化合物
B.元素⑦的气态氢化物稳定性比元素④的气态氢化物稳定性弱
C.元素①⑧形成的化合物具有两性
D.上表8种元素中,元素③的最高价氧化物对应水化物的碱性最强
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高一上学期期末考试化学试卷 题型:选择题
下表为短周期元素①~⑧的部分性质。
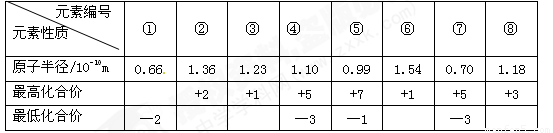
下列说法正确的是
A.元素④⑤形成的化合物是离子化合物
B.元素⑦的气态氢化物稳定性比元素④的气态氢化物稳定性弱
C.元素①⑧形成的化合物具有两性
D.上表8种元素中,元素③的最高价氧化物对应水化物的碱性最强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com