
| A、HR溶液的导电性较弱,HR属于弱酸 |
| B、某化合物溶于水导电,则该化合物为电解质 |
| C、根据电解质在其水溶液中能否完全电离,将电解质分为强电解质和弱电解质 |
| D、食盐是电解质,食盐的水溶液也是电解质 |


科目:高中化学 来源: 题型:
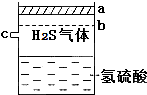 已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.
已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量的铁在氯气中燃烧可生成氯化亚铁 |
| B、向Fe(NO3)2溶液加入盐酸,由于酸性增强抑制Fe2+的水解,使c(Fe2+)增大 |
| C、Fe和Fe2O3的混合物溶于盐酸中,再加入KSCN溶液,溶液一定变为血红色 |
| D、把一定量的铁和铜的混和粉未投入到FeCl3溶液中,不可能出现只有铁剩余没有铜剩余的情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熵变小于零而焓变大于零的反应肯定不能发生 |
| B、用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度维持25℃不变,溶液中各离子浓度均减小 |
| C、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ/mol,则H2燃烧热为241.8 kJ/mol |
| D、已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2;则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
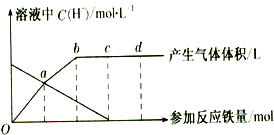
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Na+、Cl- |
| B、Na+、H+、NO3-、SO42- |
| C、Fe3+、Na+、Cl-、SO42- |
| D、K+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙与盐酸反应:CO32-+2H+=CO2+H2O |
| B、硫酸钠溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
| C、硝酸银溶液与盐酸反应:Ag++Cl-=AgCl↓ |
| D、氧化铜与稀硫酸反应:CuO+2H+═Cu2++H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com