
【题目】配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因可能是 ( )
A. 容量瓶中原有少量蒸馏水
B. 称量药品时间过长
C. 定容时俯视液面
D. 洗涤烧杯和玻棒的溶液转入容量瓶中;
科目:高中化学 来源: 题型:
【题目】研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
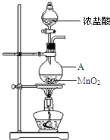
(1)仪器A的名称为_________;A中反应的离子方程式为______________________;
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | ____________________________ |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为______________________;
②不能证明产生的气体中含有HCl的实验是______________(填字母序号);
(3)已知将HCl气体通入饱和食盐水中有白色固体析出.乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因______________;
(4)已知:2S2O32-+I2═S4O62-+2I-.丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl.
I.测定X中溶解的Cl2.取25.00mL溶液X,加入过量KI溶液,然后用0.04molL-1 Na2S2O3溶液滴定生成
的I2,达滴定终点时消耗Na2S2O3溶液V mL.
Ⅱ.测定X中Cl元素总量.另取25.00mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10molL-1 AgNO3溶液滴定所得溶液中的Cl-.
①X中的HClO不会影响I的测定结果,原因是_________________________;
②由I、Ⅱ中实验数据可证明A中产生的气体中含有HCl,则Ⅱ中消耗0.10molL-1 AgNO3溶液的体积应大于____________________mL(用含V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的应用极为广泛。利用如下图所示原电池可测量空气中Cl2的含量,其中电解质是Ag+可以自由移动的固体物质,下列分析正确的是
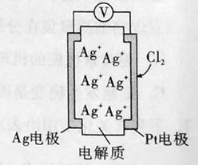
A.电流经外电路从Ag流向Pt电极
B.电池工作时,电解质中Ag+数目增多
C.正极反应:Cl2+2e-=2Cl-
D.空气中c(Cl2)越大,Ag极消耗速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是常见的有机物质,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平。有关物质的转化关系如图所示,请回答下列问题:

(1)B的结构式为 。D的物质的名称是 。
(2)在①~④反应中,属于加成反应的是 (填反应序号)。
(3)写出下列反应的化学方程式:
反应① ;反应② ;反应③ 。
(4)实验室用下图所示装置进行反应④。

A.反应④的化学方程式是 。
B.试管乙中应加入 ,乙中的导管不能伸入到液面下的原因是 。
C.实验完成后,从试管乙中分离出有机物C的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
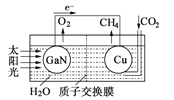
(1)科学家用氮化镓材料与铜组装如右图的人工光合系统, 利用该装置成功地实现了以CO2和H2O合成CH4。
①写出铜电极表面的电极反应式 。
②为提高该人工光合系统的工作效率,可向装置中加入少量 (选填“盐酸”或“硫酸”)。
(2)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式 。
(3)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g) 。
2CO(g)+2H2(g) 。
①该反应的平衡常数表达式为 。
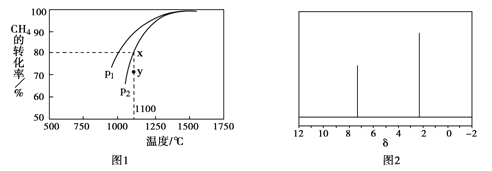
②在密闭容器中通入物质的量浓度均为0.1mol·L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示,则压强P1 P2(填“>”或“<”);压强为P2时,在Y点:v(正) v(逆)(填“>”、“<”或“=”)。
(4)天然气也可重整生产化工原料,最近科学家们利用天然气无氧催化重整获得芳香烃X。由质谱分析得X的相对分子质量为106,其核磁共振氢谱如下图2,则X的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com