
 =
=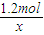 ,解得x=0.3mol,
,解得x=0.3mol,

 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2011-2012学年山东省泰安市高三上学期期中考试化学试卷 题型:选择题
把0.6mol铜粉投入含0.8mol硝酸和0.2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为
A.0.2 mol B.0.3 mol C.0.4 mol D.0.5mol
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.2 mol | B.0.3 mol | C.0.4 mol | D.0.5mol |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省泰安市高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com