
| A. | ②③ | B. | ③ | C. | ①④ | D. | ①②③ |
分析 四种短周期元素的离子aXm+、bYn+、cZn-和dRm-具有相同的电子层结构,则a-m=b-n=c+n=d+m,若m>n,故原子序数大小顺序是:a>b>c>d,结合离子所得电荷可知,X、Y为金属元素,Z、R为非金属元素,且X、Y位于Z和R的下一周期,在同一周期元素中,元素的非金属性随着原子序数的增大而增强,元素的金属性随着原子序数的增大而减小,元素的金属性越强,其最高价氧化物的水化物碱性越强,据此答题.
解答 解:四种短周期元素的离子aXm+、bYn+、cZn-和dRm-具有相同的电子层结构,则a-m=b-n=c+n=d+m,若m>n,故原子序数大小顺序是a>b>c>d,结合离子所得电荷可知,X、Y为金属元素,Z、R为非金属元素,且X、Y位于Z和R的下一周期,
①离子aXm+、bYn+具有相同的电子层结构,则离子具有相同的电子数,即a-m=b-n,则a-b=m-n,故①正确;
②由题意可知,具有相同的电子层结构,根据阴前阳后,X、Y在下一周期,Z、R在上一周期,若m>n,则Y在X的前面,R在Z的前面,所以元素的原子序数为a>b>c>d,故②错误;
③X、Y为同一周期金属元素,在同一周期元素金属性从左向右逐渐减弱,即金属性:X<Y,故③错误;
④四种主族元素中X、Y为下一周期的金属元素,且元素的原子序数a>b,在同一周期元素的金属性从左向右在减弱,即金属性Y>X,则最高价氧化物对应水化物碱性Y>X,故④正确;
故选C.
点评 本题考查学生利用离子的电子层结构相同来分析元素的位置及性质,题目中等难度,答题时注意元素周期律的灵活运用,侧重于考查学生的分析能力和对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | CS2分子中σ键与π键的数目之比是2:1 | |
| B. | 分子中含有非极性键,该分子一定是非极性分子 | |
| C. | NaOH是含有非极性共价键的离子化合物 | |
| D. | 在元素周期表中,d区和ds区的元素都是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C3H8与C9H20的两种有机物一定互为同系物 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 两个相邻同系物的相对分子质量数值一定相差14 | |
| D. | 分子组成相关一个或几个CH2原子团的化合物必定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
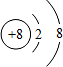 ,DE2的电子式
,DE2的电子式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
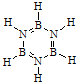 ,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:
,通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得.A在一定条件下通过多步去氢可最终转化为氮化硼(BN).请回答:| 化学键 | B-H | B-O | B-B |
| 键能(KJ•mol-1) | 389 | 561 | 293 |
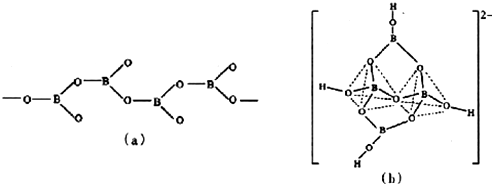
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 某烃的分子式为C6H10,用热的KMnO4溶液氧化后得到HOOCCH2CH2CH2CH2COOH,由此推断该烃的结构可能的结构简式:
某烃的分子式为C6H10,用热的KMnO4溶液氧化后得到HOOCCH2CH2CH2CH2COOH,由此推断该烃的结构可能的结构简式: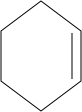 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com