
| A. | 用CH3COOH 溶液做导电性实验,灯泡很暗,能证明 CH3COOH 是弱电解质 | |
| B. | 将Ca(OH)2的饱和溶液加热,pH 和 Kw均增大 | |
| C. | 25℃时,1.0×10-3mol•L-1盐酸的pH=3.0,1.0×10-8 mol•L-1盐酸的pH=8.0 | |
| D. | 向pH相同的氨水和氢氧化钠溶液中分别加入适量NH4Cl(s)后,两溶液的pH均减小 |
分析 A.溶液的导电性与离子浓度有关;
B.将Ca(OH)2的饱和溶液加热,溶解度减小;
C.常温下,酸的pH一定小于7;
D.铵根离子会抑制一水合氨的电离,氯化铵与氢氧化钠反应生成一水合氨.
解答 解:A.0.1 mol•L-1CH3COOH溶液做导电性实验,灯光较暗,说明该醋酸中离子浓度降低,但不能说明醋酸部分电离,所以不能证明醋酸是弱电解质,故A错误;
B.将Ca(OH)2的饱和溶液加热,溶解度减小,氢氧根离子浓度减小,所以pH减小,升高温度水的离子积增大,即Kw增大,故B错误;
C.常温下,1.0×10-3 mol•L-1盐酸的pH=3,1.0×10-8 mol•L-1盐酸的pH<7,故C错误;
D.向pH相同的氨水和氢氧化钠溶液中分别加入适量NH4Cl(s)后,铵根离子会抑制一水合氨的电离,氨水的pH减小,氯化铵与氢氧化钠反应生成一水合氨,溶液中氢氧根离子浓度减小,则pH减小,故D正确.
故选D.
点评 本题考查了强弱电解质判断、影响水的离子积的因素、pH的计算等,题目难度中等,明确强弱电解质根本区别、pH的计算方法是解本题关键,侧重于考查学生的分析能力和计算能力.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:解答题
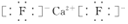 ;Y2与NaOH溶液反应的产物之一是OY2,该反应的离子方程式为2F2+2OH-=OF2↑+2F-+H2O.
;Y2与NaOH溶液反应的产物之一是OY2,该反应的离子方程式为2F2+2OH-=OF2↑+2F-+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
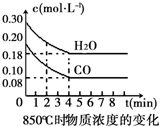 在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)浓度变化如图
在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O(g)浓度变化如图| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0J062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
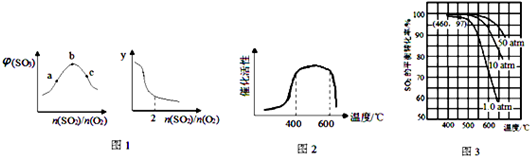
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol任何物质所含有的原子数都相同 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 | |
| D. | 国际上规定,0.012 kg C中所含有的碳原子数目为1摩 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 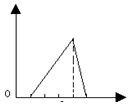 | C. | 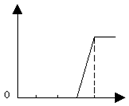 | D. | 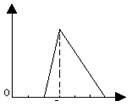 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com