
A、TNT的结构简式为: |
B、苯乙醛的结构简式为: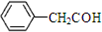 |
C、丙烷分子的球棍模型为: |
| D、乙烯的结构简式为:CH2CH2 |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
| A、钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B、HCl溶液与NaOH溶液反应:H++OH-=H2O |
| C、石灰石溶于盐酸中:CO32-+H+=CO2↑+H2O |
| D、Zn与H2SO4溶液反应:Zn+2H+=Zn2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、遇苯酚显紫色的溶液:I-、AlO2-、SCN-、Mg2+ |
| B、pH=12的溶液:AlO2-、ClO-、SO32-、Na+ |
| C、含较多Al3+离子的溶液:Na+、NO3-、S2-、AlO2- |
| D、pH=2的HNO3溶液:Na+、Ag+、NO3-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L已烷中共价键数目为19NA |
| B、26g乙炔与苯的混合物中所含量碳原子数为0.2 NA |
| C、在标准状况下,2.24L乙炔中的σ键数为0.3 NA |
| D、1 mol苯加氢气加成最多需要氢分子数为6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X2YZ3 |
| B、X2YZ4 |
| C、XYZ4 |
| D、XYZ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )| A、a和b不连接时,铁片上会有金属铜析出 |
| B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu |
| C、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D、a和b用导线连接时,可形成原电池,其中阳离子向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素A | s电子总数是p电子总数的2倍 |
| 元素C | 某种核素原子的质量数为18,中子数为10 |
| 元素X | 单质是良好的半导体材料 |
| 元素Y | 其单质为淡黄色晶体,常用来处理打碎的水银温度计 |
| 元素Z | 3d能级上有4个未成对电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com