
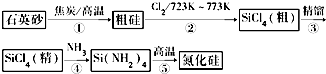
分析 根据题中反应流程可知,石英砂在高温下被碳还原得到粗硅,粗硅与氯气反应生成粗四氯化硅,精馏后得到较纯的四氯化硅,四氯化硅在高温下与氨反应生成四氨基硅,四氨基硅高温下生成氮化硅,
(1)石英砂主要成分是二氧化硅,二氧化硅与强碱反应生成可溶性硅酸盐;
(2)氧化还原反应必须有化合价的变化,据此判断;
(3)SiCl4在潮湿的空气中剧烈水解,产生白雾,说明有氯化氢产生,根据元素守恒可写出反应方程式;
(4)依据原子个数守恒判断氮化硅的化学式;
(5)根据质量守恒可知四氯化硅和氮气在氢气的气氛保护下,加强热发生反应,除生成氮化硅外还有氯化氢生成.’
解答 解:根据题中反应流程可知,石英砂在高温下被碳还原得到粗硅,粗硅与氯气反应生成粗四氯化硅,精馏后得到较纯的四氯化硅,四氯化硅在高温下与氨反应生成四氨基硅,四氨基硅高温下生成氮化硅,
(1)石英砂主要成分是二氧化硅,二氧化硅与强碱氢氧化钠溶液反应生成可溶性硅钠和水,反应的化学方程式为:SiO2+2NaOH═Na2SiO3+H2O;
故答案为:SiO2+2NaOH═Na2SiO3+H2O;
(2)①石英砂到粗硅,硅元素化合价降低,属于氧化还原反应,故选;
②粗硅与氯气反应生成四氯化硅,硅元素化合价升高,属于氧化还原反应,故选;
③四氯化硅精馏属于物理变化,故不选;
④四氯化硅与氨气反应,不存在化合价的变化,不是氧化还原反应,故不选;
⑤Si(NH2)4高温生成氮化硅,没有化合价的变化,不是氧化还原反应,故不选;
故选:①②;
(3)SiCl4在潮湿的空气中剧烈水解,产生白雾,说明有氯化氢产生,反应方程式为SiCl4+3H2O═4HCl↑+H2SiO3↓,
故答案为:SiCl4+3H2O═4HCl↑+H2SiO3↓;
(4)3mol Si(NH2)4和在高温下加热可得1mol氮化硅粉末和8mol A气体,依据原子个数守恒可知,氮化硅含有4氮原子和3个硅原子,化学式:Si3N4;
故答案为:Si3N4;
(5)四氯化硅和氮气在氢气的气氛保护下,加强热发生反应,可得较高纯度的氮化硅以及氯化氢,方程式为:3SiCl4+2N2+6H2$\frac{\underline{\;高温\;}}{\;}$Si3N4+12HCl,
故答案为:3SiCl4+2N2+6H2$\frac{\underline{\;高温\;}}{\;}$Si3N4+12HCl.
点评 本题主要考查了硅及其化合物知识,熟悉硅及其化合物的化学性质是解题关键,注意氧化还原反应的判断依据:是否有化合价的变化,题目难度不大.


科目:高中化学 来源: 题型:解答题
 某学习小组为探究部分元素化合物的性质,设计了下面的实验装置:
某学习小组为探究部分元素化合物的性质,设计了下面的实验装置:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知苯甲酸乙酯的沸点为213℃(在此温度以下水、乙醇和环己烷以7.0%、17.0%、76.0%的比例成为蒸汽逸出).请回答上述实验室制备苯甲酸乙酯的有关问题:
已知苯甲酸乙酯的沸点为213℃(在此温度以下水、乙醇和环己烷以7.0%、17.0%、76.0%的比例成为蒸汽逸出).请回答上述实验室制备苯甲酸乙酯的有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 二氧化氯泡腾片,有效成分(ClO2)是一种高效、安全的杀菌、消毒剂.
二氧化氯泡腾片,有效成分(ClO2)是一种高效、安全的杀菌、消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中含D物质的量至少为0.45 mol | |
| B. | A的平均反应速率是0.010 mol•L-1•s-1 | |
| C. | 容器中A、B、C、D的物质的量之比一定是4:5:4:6 | |
| D. | 容器中A的物质的量一定增加了0.30 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学校化学兴趣小组以在不同的温度下淀粉遇碘变蓝色的快慢为背景来研究温度对化学反应速率影响.具体研究过程:
某学校化学兴趣小组以在不同的温度下淀粉遇碘变蓝色的快慢为背景来研究温度对化学反应速率影响.具体研究过程:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,试写出:
,试写出: .
. .
. .
. ,
, ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图1配制250mL0.10mol•L-1盐酸 | B. | 图2稀释浓硫酸 | ||
| C. | 图3称量氯化钠固体 | D. | 图4CCl4萃取碘水的分液操作 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com