
【题目】可逆反应2NO2![]() 2NO+O2在定容密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在定容密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②单位时间内生成nmolO2的同时生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:l的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A、①④⑥ B、②③⑤ C、①③④ D、①②③④⑤⑥
【答案】A
【解析】
试题分析:①单位时间内生成nmolO2的同时生成2nmolNO2,表示反应速率的方向相反,且满足速率之比是相应的化学计量数之比,说明反应达到平衡状态;②单位时间内生成nmolO2的同时生成2nmolNO均表示正反应方向的速率,不能说明反应达到平衡状态;③反应速率之比是相应的化学计量数之比,所以用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:l的状态不能说明反应达到平衡状态;④颜色深浅和浓度有关系,因此混合气体的颜色不再改变的状态说明反应达到平衡状态;⑤密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此混合气体的密度不再改变的状态不能说明反应达到平衡状态;⑥混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,所以混合气体的平均相对分子质量不再改变的状态可以说明反应达到平衡状态,答案选A。


科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)![]() Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )
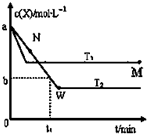
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)=(a—b)/t1 mol/(L.min)
C.M点的正反应速率v正大于N点的逆反应速率V逆
D.M点时再加入一定量的X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015新课标Ⅰ卷理综化学】我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指( )
A.氨水 B. 硝酸 C.醋 D.卤水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下表中各项的排布规律,按此规律排布第16项应为( )
1 | 2 | 3 | 4 | 5 | 6 | … |
C2H4 | C2H6 | C2H6O | C3H6 | C3H8 | C3H8O | … |
A.C6H14B.C7H14C.C7H16D.C7H16O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NO 为阿伏加德罗常数,下列说法正确的是
A、250C时,15g乙烷气体中含3.5NO 个共价键
B、标准状况下,22.4L苯在Fe 催化条件下可与NO 个Br2 发生取代反应
C、18g2H2O中含有电子数为10NO
D、1mol N2和3mol H2发生反应N2(g)+3H2(g)![]() 2NH3(g),共有6NO 个电子转移
2NH3(g),共有6NO 个电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某强酸性溶液X可能含有A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-中的一种或几种,取该溶液进行连续实验,实验过程如下:
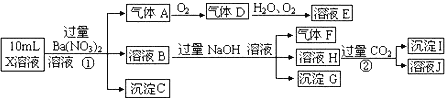
根据以上信息,回答下列问题:
上述离子中,溶液X中除H+外还肯定含有的离子是__________
请设计简单的实验检验不能确定是否含有的离子(若不止一种,可任选一种)的存在:
写出反应①的离子方程式 ;
④假设测定A、F、I均为0.1mol,100mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有 .
(2)实验室常见的几种气体发生装置如图A、B、C所示:
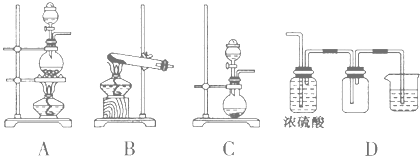
①实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为 。
②气体的性质是选择气体收集方法的主要依据.下列气体的性质与收集方法无关的是 (填序号,下同).
A.密度 B.颜色 C.溶解性 D.热稳定性 e.与氧气反应
③若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的 (填序号).
A.CO2 B.NO C.Cl2 D.H2 e.HCl
其中在D装置中连接烧杯的目的是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯丙醇是一种无色有刺激性气味的液体,是重要的有机合成原料,其结构简式为 CH2=CH—CH2OH。请回答:
(1)烯丙醇中除碳碳双键外还含有的官能团是 (名称)。
(2)0.1mol 烯丙醇与足量金属钠反应,能生成氢气 L(标准状况下)。
(3)写出烯丙醇与溴水反应的化学方程式 ,
(4)烯丙醇与CH3CO18OH发生酯化反应的化方程式为 ,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式为 。
(5)烯丙醇的一种同分异构体能发生银镜反应,其结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL0.1mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是

A. a点时溶液中所含主要溶质为(NH4)2SO4
B. a→b段发生反应的离子方程式是 SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C. b点为最大沉淀量,对应的纵坐标值为0.02
D. c点加入Ba(OH)2溶液的体积为200 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com