
【题目】为探究黑色固体 X(仅含两种元素)的组成和性质,设计并完成如下实验:
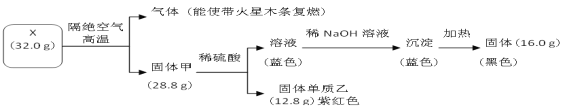
(1)X的化学式是________________。
(2)写出固体甲与稀硫酸反应的离子方程式________________________。
【答案】CuO Cu2O+2H+=Cu+Cu2++H2O
【解析】
根据框图逆推本题:气体能使带火星的木条复燃,说明隔绝空气加热会产生氧气;固体甲遇到硫酸产生蓝色溶液和紫红色固体单质乙,说明有铜产生,进而说明X中含有铜元素和氧元素,再根据质量守恒进行解答。
(1)32.0gX隔绝空气加热分解放出的能使带火星的木条复燃的气体为氧气,质量为32.0g-28.8g=3.2g,证明X中含氧元素,28.8g固体甲和稀硫酸溶液反应生成蓝色溶液,说明含铜离子,证明固体甲中含铜元素,即X中含铜元素,铜元素和氧元素形成的黑色固体为CuO,所以X为氧化铜,本题答案: CuO;
(2)由n(CuO)=32.0g÷80gmol-1=0.4mol,结合质量守恒得到n(O2)=3.2g÷32gmol-1=0.1mol,由氧元素守恒得到甲中n(Cu): n(O)=0.4mol:(O.4mol-0.1mol×2)=2:1,固体甲的化学式为Cu2O,加稀硫酸后,产生蓝色溶液和固体单质乙,固体单质乙为Cu,蓝色溶液为硫酸铜,与稀硫酸反应的离子方程式为:Cu2O+2H+=Cu+Cu2++H2O;答案:Cu2O+2H+=Cu+Cu2++H2O。


科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是
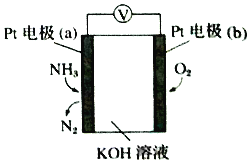
A. O2在电极b上发生还原反应
B. 溶液中OH-向电极a移动
C. 正极的电极反应式为O2+4e-+4H+=2H2O
D. 负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写错误的是
A. MgCl2=Mg2++2Cl B. NaOH=Na++O2+H+
C. HCl=H+ +Cl D. K2SO4=2K++SO42
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.10 mol·L-1的NaOH溶液,整个过程中溶液pH变化的曲线如图所示。下列叙述中正确的是

A. 点①所示溶液中:c(H+)=c(Cl-)+c(HClO)+c(OH-)
B. 点②所示溶液中:c(H+)>c(Cl-)>c(ClO—)>c(HClO)
C. 点③所示溶液中:c(Na+)=2c(ClO-)+c(HClO)
D. 点④所示溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是_____________________________________________,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是______________________________。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中______。
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解气态产物的装置:

丙组同学的实验装置中,依次连接的合理顺序为A→ _______;其中仪器F的名称___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 56 g Fe 与1mol Cl2充分反应,转移的电子数为3NA
B. 分子数为 0.1NA的CH4和NH3混合气体,含有的共用电子对数为0.4NA
C. 25℃时,1L pH=12的Ba(OH)2溶液中含有0.02NA 的OH-
D. 常温常压下,22 g D3O+中含有10NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常见的混合物分离或提纯的基本装置如下:
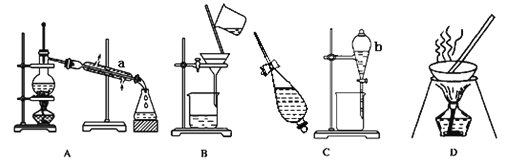
(1)写出仪器名称:a___________,b__________。
(2)从海带提取碘的操作如下,除特殊说明外,请在空白处填上装置中的序号:将干海带进行灼烧,海带灰中含有较多KI,将海带灰溶于水,然后__________得到澄清滤液;向滤液中加入硫酸和H2O2混合溶液,得到棕褐色含有单质碘的水溶液。该反应的离子方程式为:__________________。向碘的水溶液中加入适量CCl4,进行___________操作将上下两层溶液分开。将含有碘的CCl4溶液置于蒸馏烧瓶内进行___________操作,可以粗略从CCl4溶液中分离出碘。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,消耗50mL 8mol/L的氢氧化钠溶液,则无水乙醇的燃烧放出的热量不可能是( )
A. 10Q B. 5Q~10Q C. 大于10Q或小于5Q D. 小于8Q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com