
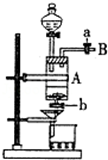
 ���Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ͬѧ�����÷���м��������ͭ���ʣ���̽���Ʊ�FeCl3•6H2O�ķ�����ͬѧ����Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ��������ϡ���ᣬʵ��ʱ�ȴ�a���ر�b���÷�Һ©����A�м�������������ַ�Ӧ����ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3•6H2O���壮
���Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ͬѧ�����÷���м��������ͭ���ʣ���̽���Ʊ�FeCl3•6H2O�ķ�����ͬѧ����Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ��������ϡ���ᣬʵ��ʱ�ȴ�a���ر�b���÷�Һ©����A�м�������������ַ�Ӧ����ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3•6H2O���壮���� ���Ŀ�����Ʊ�FeCl3•6H2O����װ��ͼ��֪����A�з���м�����ᷴӦ�����Ȼ������������˿ɷ����ͭ���Ȼ��������������������ձ��У����Ὣ�Ȼ��������������Ȼ�����������Ũ����ӦҺ������������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3•6H2O���壬
��1���������ܽ�ɽ����γ�ԭ���ʹ��Ӧ���ʼӿ죻
��2��ϡHNO3��ǿ�����ԣ�ʹFe2+ ȫ��������Fe3+��
��3����֤��������ѹǿ��ȣ�ʹ��Һ©���е���ɵ���A�У�
��4�����Ȼ���������Ϊ�Ȼ�����ͬʱ�����������ʣ���ѡ����ɫ�������������һĿ��
��� �⣺ʵ���Ŀ�����Ʊ�FeCl3•6H2O����װ��ͼ��֪����A�У�����м�����ᷴӦ�����Ȼ������������˿ɷ����ͭ���Ȼ��������������������ձ��У����Ὣ�Ȼ��������������Ȼ�����������Ũ����ӦҺ������������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3•6H2O���壬
��1������м��������ͭ���ʣ��������Cu�����γ�Fe-Cuԭ���ʹ��Ӧ���ʼӿ죬
�ʴ�Ϊ������м�еIJ�����������Fe�������й���ԭ��أ��ӿ��˷�Ӧ���ʣ�
��2��������ϡHNO3��֤ʹFe2+ ȫ��������Fe3+����Ӧ�����ӷ���ʽ�ǣ�3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
�ʴ�Ϊ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
��3������ʵ������У����ɼ�a���������װ���������ͬ��ʹ��Һ©���е���ɵ���A�У�
�ʴ�Ϊ��ʹװ���ڲ�����������ͨ������A��Һ�����£�
��4�����Ȼ���������Ϊ�Ȼ�����ͬʱ�����������ʣ�����ѡ���������������ϡ���ᣬ����˫��ˮ��
�ʴ�Ϊ���٢ڣ�
���� ���������ú�ͭ�ķ���м�Ʊ�FeCl3•6H2O��ʵ��̽�����������Ʊ���������ƣ��漰��Fe2+����������Һ�������ᾧ��Fe3+�ķ�ˮ�⣬����������ԭ������۽��ʹ���û�з���м�ܽ����ʿ��ԭ������������ѧ���ķ�����������������ѧʵ��������


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� 0.1 mol/L�İ�ˮ�м���������粒��壬����Һ��$\frac{c��O{H}^{-}��}{��N{H}_{3}•{H}_{2}O��}$���� | |
| B�� | �����£�0.1 mol/LһԪ�ᣨHA����Һ�� pH=3�������Һ�У�c2��H+��=c��H+����c��A-��+Kw | |
| C�� | ���� 1 mol KAl��SO4��2 ����Һ�м��� Ba��OH��2 ��Һ�õ����������ʵ������Ϊ 2 mol | |
| D�� | �� Ca��ClO��2��Na2SO3��FeCl3��NaAlO2 ��Һ���ɾ��ò���ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��CO2 | B�� | ͨ��NH3 | C�� | ��ȴĸҺ | D�� | ����ʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
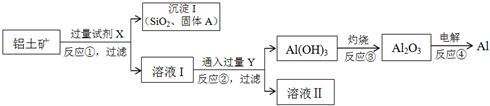
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol/L NaHCO3��Һ��0.1 mol/L NaOH��Һ�������ϣ�������Һ�У�c��Na+����c��CO32-����c��HCO3-����c��OH-�� | |
| B�� | 20 mL 0.1 mol/L CH3COONa��Һ��10 mL 0.1 mol/L HCl��Һ��Ϻ���Һ�����ԣ�������Һ�У�c��CH3COO-����c��Cl-����c��CH3COOH����c��H+�� | |
| C�� | �����£�pH=2��������pH=12�İ�ˮ�������ϣ�������Һ�У�c��Cl-��+c��H+����c��NH4+��+c��OH-�� | |
| D�� | 0.1 mol/L CH3COOH��Һ��0.1 mol/L NaOH��Һ�������ϣ�������Һ�У�c��OH-����c��H+��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
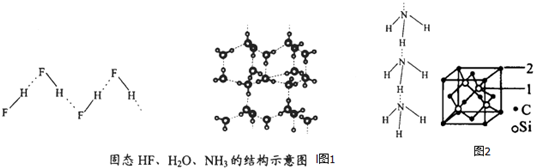
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ���X-H��Y | ����kJ•mol-1 |
| ��HF��n | D-H��F | 28.1 |
| �� | O-H��O | 18.8 |
| ��NH3��n | N-H��N | 5.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �������м����Ҵ���ֵ�ı� | |
| B�� | �ո�ȼ�������������ԭ��֮һ | |
| C�� | �����������ķ������Ա������� | |
| D�� | ���г��ּ�������Ҫ�ǵ绯ѧ��ʴ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���� | ���� |
| A | T��ʱ����NaCl��NaBr�Ļ�� ��Һ�еμ�AgNO3��Һ | �ȳ��ְ�ɫ���� | T��ʱ��Ksp�� AgCl��AgBr |
| B | ���Ũ�ȵ�Na2CO3��Һ��Na2SO4 ��Һ�еμӷ�̪�Լ� | Na2CO3��Һ���ɫ��Na2SO4 ��Һ���������� | �ǽ����ԣ�S��C |
| C | �����£�ȡ����CaSO4��Һ����� ��Һ��������ʵ�� | ����ʵ��ĵ��ݽ��� | CaSO4�ʹ���� Ϊ������� |
| D | ��Ʒ����Һ�еμ�NaClO��Һ ��ͨ��SO2���� | Ʒ����Һ����Ϊ��ɫ | ���߾���Ư���� ��ԭ����ͬ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | LiH�����Ӿ��� | B�� | LiH��ˮ��Һ������ | ||
| C�� | LiH��һ�������� | D�� | LiH��H-�뾶����Li+�뾶 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com