
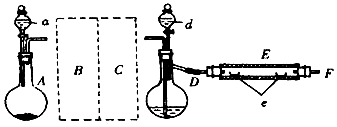
| A. |  实验室中制取少量乙酸乙酯 | B. | 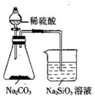 比较非金属性S>C>Si | ||
| C. | 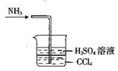 处理尾气 | D. |  闭合开关K形成原电路 |
分析 A.乙酸乙酯与NaOH反应;
B.发生强酸制取弱酸的反应,可知酸性硫酸>碳酸>硅酸;
C.四氯化碳可隔绝氨气与水;
D.关闭K,构成原电池,Zn为负极,Cu为正极.
解答 解:A.小试管在应为饱和碳酸钠溶液,且导管应在液面上防止倒吸,故A错误;
B.发生强酸制取弱酸的反应,可知酸性硫酸>碳酸>硅酸,则非金属性S>C>Si,故B正确;
C.四氯化碳可隔绝氨气与水,图中装置可防止倒吸,故C正确;
D.关闭K,构成原电池,Zn为负极,Cu为正极,则闭合开关K形成原电路,故D正确;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、酸性比较、物质的制备、原电池、实验技能为解答的关键,侧重分析与实验能力的考查,注意化学实验方案的评价,题目难度不大.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 8.4gNaHCO3晶体中含有0.1NA个CO32- | |
| B. | 常温常压下,32g臭氧所含的氧原子数为2NA | |
| C. | 0.1molFe与过量硝酸反应,转移电子数为0.2NA | |
| D. | 1molCH4与1molCl2在光照下反应,生成CH3Cl的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 根据所学知识完成下列填空.
根据所学知识完成下列填空.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
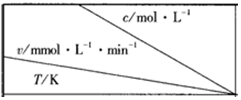 | 0.600 | 0.500 | 0.400 | a |
| 318.2 | 3.60 | c | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | d | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A. | a<0.400 | B. | c>2.40 | C. | b<318.2 | D. | d<1.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 操 作 | 现 象 |
| 取0.1mol/L的FeBr2溶液100mL,测溶液的pH | pH试纸变红(约为4) |
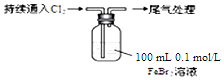 | ⅰ.开始通入100mLCl2(折合标准状况),溶液由浅绿色逐渐变黄; ⅱ.稍后,继续通入Cl2,溶液黄色加深,变为棕黄色; iii.稍后,溶液由棕黄色变浅,最终变为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同 | |
| B. | 铜导线替换盐桥,原电池仍继续工作 | |
| C. | 开始时,银片上发生的反应是Ag-e-═Ag+ | |
| D. | 电子通过盐桥从乙池流向甲池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2N2O5═4NaNO3+O2↑ | B. | Na2O2+2NO2═2NaNO2+O2 | ||
| C. | Na2O2+N2O4═2NaNO3 | D. | 2Na2O2+2Mn2O7═4NaMnO4+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
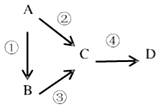 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如下转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如下转化关系,其中A是单质.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com