


分析 制备CuSO4•5H2O及CaCO3步骤:孔雀石主要成分Cu2(OH)2CO3,其中还含少量Fe、Si的化合物.铁元素以+2、+3价存在,孔雀石与硫酸反应中,少量Fe的氧化物均与硫酸反应,只有SiO2不反应,溶液A中含Cu2+、Fe2+、Fe3+,由工艺流程转化关系可知,实现由溶液A至溶液B转化,目的是将Fe2+氧化为Fe3+,试剂①应为氧化剂,且不能引入新的杂质,则溶液B中含Cu2+、Fe3+,加CuO促进铁离子水解转化为沉淀,所以溶液C中主要为硫酸铜,蒸发浓缩、冷却结晶得到CuSO4•5H2O;制备CaCO3时,先通入氨气,增大二氧化碳的溶解,生成碳酸铵与氯化钙反应生成碳酸钙、氯化铵,则过滤可得到CaCO3,以此来解答.
(1)为使Fe2+、Fe3+一起沉淀,选择合适的氧化剂将Fe2+氧化而又不引入新杂质;检验Fe3+,选择特征试剂KSCN;
(2)从溶液中要析出晶体,采用冷却结晶法;过滤时要用到玻璃棒引流;
(3)CaCl2溶液不能与CO2反应,加入碱能反应,但又不能引入杂质,应通入NH3(或先加入NH3•H2O);氨气极易溶于水,要注意防倒吸,a装置广口瓶内的进气管长,容易倒吸,c装置中的倒置漏斗、d中的多空球泡不可以防倒吸;
解答 解:制备CuSO4•5H2O及CaCO3步骤:孔雀石主要成分Cu2(OH)2CO3,其中还含少量Fe、Si的化合物.铁元素以+2、+3价存在,孔雀石与硫酸反应中,少量Fe的氧化物均与硫酸反应,只有SiO2不反应,溶液A中含Cu2+、Fe2+、Fe3+,由工艺流程转化关系可知,实现由溶液A至溶液B转化,目的是将Fe2+氧化为Fe3+,试剂①应为氧化剂,且不能引入新的杂质,则溶液B中含Cu2+、Fe3+,加CuO促进铁离子水解转化为沉淀,所以溶液C中主要为硫酸铜,蒸发浓缩、冷却结晶得到CuSO4•5H2O;制备CaCO3时,先通入氨气,增大二氧化碳的溶解,生成碳酸铵与氯化钙反应生成碳酸钙、氯化铵,反应为:CaCl2+CO2+2NH3•H2O=CaCO3↓+2NH4Cl+H2O,则过滤可得到CaCO3.
(1)本实验要除去Fe2+、Fe3+等离子,先加入合适的氧化剂时不能引入新的杂质,可加入H2O2,发生的反应为:2Fe2++H2O2+2H+=2Fe3++2H2O,因Fe3+遇KSCN溶液变为血红色,则可用KSCN检验Fe3+;
故答案为:c;2Fe2++H2O2+2H+=2Fe3++2H2O;d;
(2)从溶液中要析出晶体,采用冷却结晶法,然后进行过滤等操作,过滤用到的仪器有烧杯、玻璃棒、漏斗、滤纸等仪器,其中玻璃棒在过滤时起到引流的作用,在蒸发时起到搅拌的作用,
故答案为:加热蒸发、冷却结晶;玻璃棒;搅拌、引流;
(3)CaCl2溶液不能与CO2反应,加入碱能反应,但又不能引入杂质,应通入NH3,发生反应为:CaCl2+CO2+2NH3•H2O=CaCO3↓+2NH4Cl+H2O,实验室收集氨气时要注意防止倒吸,因为氨气极易溶于水,吸收时导管不能插入到液面以下,可用倒置的漏斗,
故答案为:NH3•H2O;CaCl2+CO2+2NH3•H2O=CaCO3↓+2NH4Cl+H2O;b;
点评 本题通过制备CuSO4•5H2O及CaCO3实验考查常见金属的单质及其化合物的应用,考查物质的制取和提纯等实验操作,注意蒸发、过滤、滴定操作的注意事项,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳分子的电子式: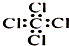 | B. | 对硝基甲苯的结构简式: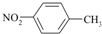 | ||
| C. | 羟基的电子式: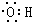 | D. | 乙醛的结构简式:CH3COH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 苯酚 | 94 | 1.0722 | 182 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 异丙苯 | 120 | 0.8640 | 153 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
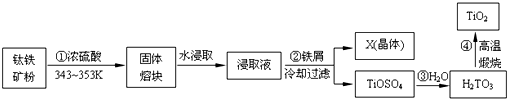
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
| 实验步骤 | 实验现象 | 实验结论 |
| ① | 溶液X中含有Na+ | |
| ② | 溶液X中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3溶于水所得溶液能导电,据此可判断NH3属于电解质 | |
| B. | 某气体只含 N、H 两种元素,且质量之比为 14:3,则该气体一定为纯净物 | |
| C. | 氨气和氯化氢气体混合后生成的NH4Cl是离子化合物,因此该反应为离子反应 | |
| D. | 尽管 NO2能与水反应生成硝酸,但 NO2不属于酸性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com