
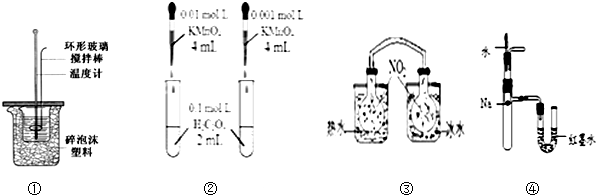
| A. | 装置①用于测定中和热装置 | |
| B. | 装置②依据褪色快慢比较浓度对反应速率的影响 | |
| C. | ③依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| D. | 装置④依据U管两边液面的高低判断Na和水反应的热效应 |
分析 A.温度计测定温度,烧杯之间的塑料可隔热;
B.只有浓度一个变量,但两种高锰酸钾的浓度不同,颜色本来就不同,不符合控制变量法;
C.温度不同,影响2NO2(g)?N2O4(g)平衡移动;
D.U管两边液面左低右高,可知Na与水的反应放热.
解答 解:A.温度计测定温度,烧杯之间的塑料,搅拌器搅拌可加速反应,可测定中和热,故A正确;
B.两种高锰酸钾的浓度不同,颜色不同,不符合控制变量法,应保证高锰酸钾浓度相同,用不同浓度的草酸来做实验,故B错误;
C.可隔热反应2NO2(g)?N2O4(g)为放热反应,放入热水中,平衡逆向移动,二氧化氮的浓度增大,颜色加深;放入冷水中,平衡正向移动,二氧化氮浓度减小,颜色变浅,故C正确;
D.钠与反应放热,大试管内气体受热膨胀,U管左侧液面下降,右侧液面上升,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及中和热测定、反应塑料、化学平衡及反应中热效应等,侧重化学反应原理和实验技能的考查,注意从装置的目的性、操作的准确性等方面评价,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应和复分解反应不可能是氧化还原反应 | |
| B. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| C. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| D. | 在氧化还原反应中肯定有一种元素被氧化,另一种元素被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
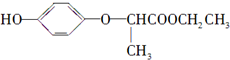 下列有关HPE的说法正确的是( )
下列有关HPE的说法正确的是( )| A. | 1 mol HPE最多可和2 mol NaOH反应 | |
| B. | HPE不能跟浓溴水反应 | |
| C. | HPE不能发生加成反应 | |
| D. | HPE在核磁共振氢谱中有6个峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸溶液反应:2H++CO32-=H2O+CO2 | |
| B. | 铁钉放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸氢钠与稀盐酸反应:HCO3-+H+=CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | m mol SO2、n mol O2、p mol SO3 |
| c(SO3)/mol•L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1mol水和1molH2的体积都约是22.4L | |
| B. | 2gH2和44gCO2的体积相等 | |
| C. | 1mol某气体的体积为22.4L,则该气体一定处于标准状况 | |
| D. | 在标准状况下,1gH2和11.2LO2的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
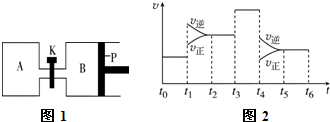
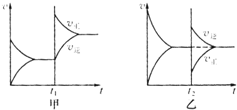 在一定条件下,有反应xA+yB?zC.
在一定条件下,有反应xA+yB?zC.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com