
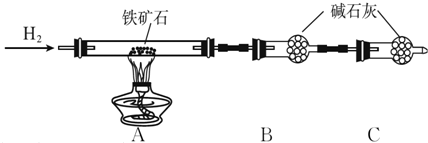
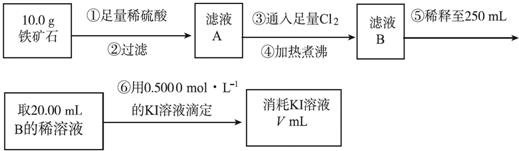
���� ��1��B�еļ�ʯ���������û���Ӧ���ɵ�ˮ�ģ�Ϊ�˷�ֹ�����ɷֶ�ʵ���Ӱ�죬Ҫ��һ��װ�����տ����е�ˮ�Լ�������̼��
��2����Ӧ��װ��B����1.35g������������������Ӧ���������������ֵ�����Ը��ݲ����������㣻
��1����п��Խ�ˮ�е�������ߣ�
��2������ϡ��Һ�������һ���������Һ��ѡ����������ش�
��3�����ݵζ������Լ��ζ������е�ʵ��������֪ʶ���ش��жϣ�
��4������Ԫ���غ�ͻ�ѧ��Ӧ����ʽ���м��㣻
������Ԫ��������������Ԫ�������������������������Ļ�ѧʽ��
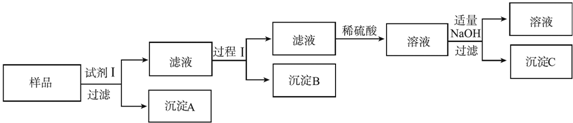
��� �⣺��1����ʵ���У���������������Ӧ���ɽ�������ˮ�����ݹ��������ı仯���������ĺ�����B���ĸ�������������ղ�����ˮ����������Cװ��Ҫ��ֹ��ֹ�����е�ˮ������CO2����B�У�Ӱ��ⶨ�����
�ʴ�Ϊ����ֹ�����е�ˮ������CO2����B�У�Ӱ��ⶨ�����
��2����ķ�Ӧ��װ��B����1.35g�����ݷ�Ӧ��ʵ�ʣ����ӵ���ˮ�����������������غ㶨�ɣ���������ʯ�����İٷֺ����ǣ�$\frac{\frac{1.35}{18}��16}{5.0}$��100%=24%��
�ʴ�Ϊ��24%��
��1��������ʯ�м������ᣬ����Ӧ���������������Һ�������ڹ�����������Һ�������������������к���Խ����������ܽ�ȣ�������Һ���ܽ�Ĺ�����Cl2��
�ʴ�Ϊ��������Һ���ܽ�Ĺ�����Cl2��
��2����ԭ��Һϡ�͵�250mL����Ҫʹ�õIJ������������У��ձ�������������ͷ�ιܡ�250mL����ƿ����ȱ��250mL����ƿ��
�ʴ�Ϊ��250mL����ƿ��
��3��a����ˮΪ��ɫ������������Ҳ�ǻ�ɫ��Һ���ζ����������ָʾ������a����
b���ζ������У����������Ժ͵����ӷ�����Ӧ�����������Ӻ͵ⵥ�ʣ��ⵥ������������Һ��ʾ��ɫ������ȷ���Ƿ�ﵽ�ζ��յ㣬��b����
c���ζ���������ˮϴ�Ӻ�����ñ�Һ��ϴ����c����
d����ƿ����Ҫ�ô���Һ��ϴ����d��ȷ��
e���ζ������У��۾�ע����ƿ����ɫ�ı仯����e����
f���ζ�������30s����Һ���ָ�ԭ������ɫ�ٶ�������f��ȷ��
�ʴ�Ϊ��df��
��4�����ݷ�Ӧ�ķ���ʽΪ2Fe3++2I-=2Fe2++I2��֪�����ĵĵ����������������ʵ�����ȣ�n��Fe3+��=n��KI��������0.4000mol•L-1��0.025L=c��Fe3+����0.02L�����c��Fe3+��=0.5mol•L-1��������Ԫ�صİٷֺ���Ϊ��$\frac{0.5mol/L��0.25L��56g/mol}{10g}$��100%=70%��
�ʴ�Ϊ��70%��
����������������70%����Ԫ�ص�����������24%������100g����ʯ�У���Ԫ�ص�������70g����Ԫ��������24g����Ԫ�غ���Ԫ�ص����ʵ�����Ϊ��$\frac{70}{56}$��$\frac{24}{16}$=5��6������������Ļ�ѧʽΪ��Fe5O6��
�ʴ�Ϊ��Fe5O6 ��
���� ���⿼����̽������ʯ����Ԫ�غ���Ԫ�صĺ����ķ����������Ǹ߿��еij������ͣ������е��Ѷȵ����⣬���ض�ѧ��������������ѵ��������������ѧ���淶�Ͻ���ʵ����ơ��������������������ۺ���ǿ�����ۺ�ʵ������ϵ���ܣ�Ҫ��ѧ���������桢ϸ�µ����⣬��ϵ��ѧ����֪ʶ�ͼ��ܣ�ȫ��ϸ�µ�˼�����ܵó���ȷ�Ľ��ۣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
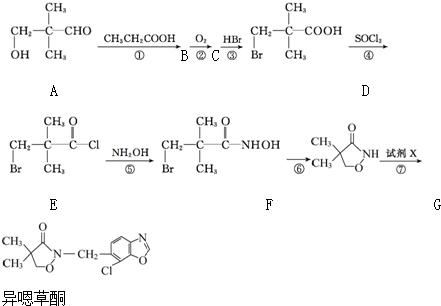
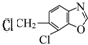 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
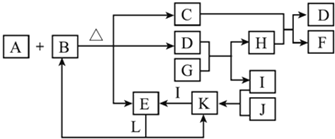
| A�� | 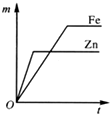 | B�� | 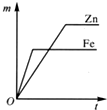 | C�� | 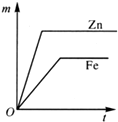 | D�� | 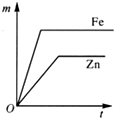 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
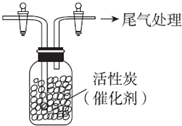 ijѧϰС������SO2���л�ԭ�ԣ��Ʋ�SO2�ܱ�Cl2��������SO2Cl2��
ijѧϰС������SO2���л�ԭ�ԣ��Ʋ�SO2�ܱ�Cl2��������SO2Cl2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
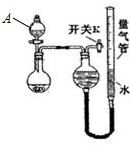 þ������п�������г��������ֽ������������ϻ��������Ϣ��
þ������п�������г��������ֽ������������ϻ��������Ϣ��| ��� | ��ĩ���� | �����ܵ�һ�ζ��� | �����ܵڶ��ζ��� |
| �� | 2.0 g | 10.0 mL | 346.2 mL |
| �� | 2.0 g | 10.0 mL | 335.0 mL |
| �� | 2.0 g | 10.0 mL | 345.8 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A��B��C��D | B�� | A��C��D��B | C�� | C��A��B��D | D�� | B��D��C��A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na | B�� | Mg | C�� | Al | D�� | Zn |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2ͨ�����ʯ��ˮ�� | B�� | ϡ�����м���ͭƬ | ||
| C�� | ϡ�����м�����м | D�� | HCl��Һ����Na2CO3��Һ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com