
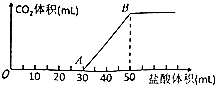
 将5.04gNa2CO3、NaOH的固体混合物加水溶解,向该溶液中逐滴加入2mol•L-1的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中不正确的是( )
将5.04gNa2CO3、NaOH的固体混合物加水溶解,向该溶液中逐滴加入2mol•L-1的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中不正确的是( )| A. | OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3- | |
| B. | B点溶液中的溶质为NaCl,其质量为5.85g | |
| C. | 当加入35mL盐酸时,产生CO2的体积为224mL(标准状况) | |
| D. | 混合物中NaOH的质量2.40g |
分析 A.OA段发生反应的离子方程式为:H++OH-═H2O CO32-+H+═HCO3-;
B.B点为NaCl溶液,n(NaCl)=n(HCl),带入m=nM计算;
C.AB段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式来求解;
D.根据AB段求出二氧化碳的物质的量,然后根据碳守恒求出碳酸钠的质量,最后根据总质量求氢氧化钠的质量.
解答 解:A.OA段发生反应的离子方程式为:H++OH-═H2O、CO32-+H+═HCO3-,故A正确;
B.B点为NaCl溶液,n(NaCl)=n(HCl)=2mol•L-1×0.05L=0.1mol,m(NaCl)=0.1mol×58.5g/mol=5.85g,故B正确;
C.AB段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,根据方程式n(CO2)=(35-30)×10-3L×2mol/L=0.01mol,所以二氧化碳的体积为:0.01mol×22.4L/mol=224mL,故C正确;
D.由反应HCO3-+H+=H2O+CO2↑,n(CO2)=n(Na2CO3)=(50-30)×10-3×2mol/L=0.04mol,所以氢氧化钠的质量为5.04g-0.04×106g=0.8g,故D错误;
故选D.
点评 本题考查混合物计算,理解判断各阶段发生的反应是关键,侧重学生分析判断和计算能力的考查,难度中等.


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸、空气、小苏打、乙醇 | B. | 生石灰、漂白粉、铁、二氧化硫 | ||
| C. | 明矾、盐酸、碳酸钙、氯气 | D. | 冰水混合物、氨水、纯碱、干冰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:P>S>Cl | B. | 最外层电子数:F<O<N | ||
| C. | 金属性:Na>Mg>Al | D. | 非金属性:Cl>Br>I |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Ⅰ操作 | Ⅱ结论 | |
| A | 滴加Ba(OH)2溶液生成白色沉淀 | 原溶液中有SO42- |
| B | 滴加AgNO3溶液生成白色沉淀 | 原溶液中有Cl- |
| C | 滴加过量浓NaOH溶液并加热,将湿润红色石蕊试纸置于试管口,试纸变蓝色 | 原溶液中有NH4+ |
| D | 滴加氯水和CCl4,振荡、静置,上层溶液显紫红色 | 原溶液中有I- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 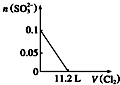 | B. | 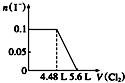 | C. | 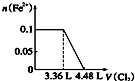 | D. | 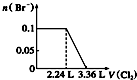 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 5 | C. | 6 | D. | 多于6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | Na2CO3可与盐酸反应 | 碳酸钠溶液可用于治疗胃酸过多 | Ⅰ对,Ⅱ对,有 |
| B | Cl2使鲜艳的红色花瓣褪色 | Cl2具有漂白性 | Ⅰ对,Ⅱ对,有 |
| C | 铝制饮具最好不要盛放酸性或碱性 较强的液体食物 | 因为Al和Al2O3既可以与酸反应, 又可以与碱反应 | Ⅰ对,Ⅱ对,无 |
| D | Na2O2能和CO2、H2O反应生成O2 | 过氧化钠可用作航天员的供氧剂 | Ⅰ对,Ⅱ对,有 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
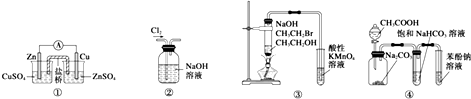
| A. | 装置①:构成锌-铜原电池 | |
| B. | 装置②:除去Cl2中含有的少量HCl | |
| C. | 装置④:由实验现象推知酸性强弱顺序为CH3COOH>H2CO3>C6H5OH | |
| D. | 装置③:验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com