
(1)下图所示是实验室中制取气体的一种简易装置。
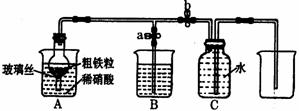
① 用下列方法检验发生装置的气密性,能否达到目的 (填能或否)
关闭止水夹a和b,从A处烧杯中加入水,使干燥管与烧杯中液面 形成液面差,一段时间后,液面差没有变化,说明气密性良好。
形成液面差,一段时间后,液面差没有变化,说明气密性良好。
②实验室利用上图所示发生装置可以制取下列 气体(双选)。
A.Cl2 B.CO2 C.H2 D.SO2
(2)利用该装置,用粗铁粒与3mol·L-1硝酸反应制取NO气体。请回答有关问题。
①NO气体能用排水法收集,而不能用排空气法收集的原因是 。
②制取NO时,向A烧杯中加入稀硝酸,B烧杯中加入NaOH溶液,同时打开止水夹a,关闭止水夹b,A装置的干燥管中观察到气体的颜色的变化为 ;B装置烧杯中NaOH溶液的作用是 。当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体。
③将a mol铁与含b molHNO3的稀溶液充分反应,反应后Fe和HNO3均无剩余,若HNO3的还原产物只有NO,则反应中被还原的硝酸的物质的量为 mol,该反应中转移电子的物质的量为 mol(均用含b的代数式表示)。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
运用化学反应原理研究卤族元素的有关性质具有重要意义。
(1)下列关于氯水的叙述正确的是________(填写序号)。
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)氯气在工业上有着极其广泛的用途。工业上通过氯碱工业生产氯气,其反应的离子方程式为________________________________。室温下,用惰性电极电解100 mL饱和食盐水,当阴极产生标准状况下11.2 mL气体,忽略溶液体积的变化时,所得溶液的pH=____________。
(3)常温下,已知25 ℃时有关弱酸的电离常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离常数 | K=4.7×10-8 | K1=4.3×10-7, K2=5.6×10-11 |
写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式________________________________________________________________________。
若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因____________________________________________________________________
________________________________________________________________________。
(4)服用含碘化钾的碘药片可抗核辐射。将碘药片剥去糖衣皮研碎后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色。完成并配平溶液由蓝色变为无色的化学反应方程式(如果化学计量数是1,不用填写):_____+______+_______―→_______HIO3+________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某一溴代烷水解后的产物在红热铜丝催化下, 最多可被空气氧化生成4种不同的醛,该一溴代烷的分子式可能是
A.C4H9Br B.C5H11Br C.C6H13Br D.C7H15Br
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于浓硝酸和浓硫酸的叙述正确的是( )
A.都是常用的干燥剂
B.常温下都能与氢前金属反应放出氢气
C.一定条件下和铜反应中都表现出强氧化性和强酸性
D.分别露置在空气中,容器内溶质的物质的量浓度都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
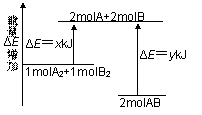
化学反应A2+B2=2AB的能量变化如图所示。下列说法正确的是( )
A.该反应是吸热反应
B.断裂1molA-A键和1mol B-B键放出xkJ能量
C.断裂2molA-B键需要吸收ykJ能量
D.2molAB的总能量高于1mol A2和1mol B2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.在FeI2溶液中滴入几滴稀溴水:Fe2+ + Br2 = 2Fe3+ + 2Br-
B. FeCl3溶液中滴加过量Na2S溶液:2Fe3++S2- ═2Fe2++S↓
C.在NaHSO3溶液中滴入Ca(OH)2溶液:HSO3- + OH- = SO32- + H2O
D.等物质的量浓度、等体积的NaHSO4溶液与Ba(OH)2溶液混合:
H+ + SO42- + Ba2+ + OH- = BaSO4↓+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室用粗硅制备四氯化硅的装置示意图。
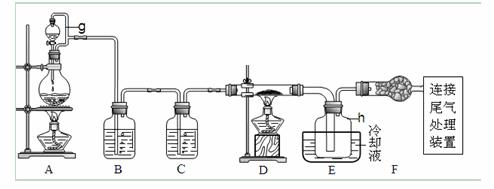
相关信息如下:①四氯化硅遇水极易水解;
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
③有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | — | 315 | — |
| 熔点/℃ | -70.0 | -107.2 | — | — | — |
| 升华温度/℃ | — | — | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式 。
(2)装置A中仪器g的名称是 ;装置C中的试剂是 ;
(3)从安全角度考虑,若将装置E中通入h瓶的粗玻璃导气管换成细玻璃导气管,可能带来的后果是 。
(4)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是 (填写元素符号)。
(5)为分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
5Fe2++MnO4-+8H+ 5Fe3++Mn2++4H2O
5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂? (填“是”或“否”),判断达到滴定终点的现象是 。
②某同学称取5.000g残留物后,经预处理后在容量瓶中配制成100 mL溶液,移取25.00mL试样溶液,用1.000×10-2 mol/L KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用下面的方案进行某些离子的检验,其中方案设计最严密的是 ( )
A.检验试液中的SO :试液
:试液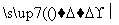 无沉淀
无沉淀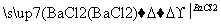 白色沉淀
白色沉淀
B.检验试液中的SO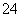 :试液
:试液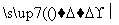 无沉淀
无沉淀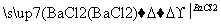 白色沉淀
白色沉淀
C.检验试液中的I-:试液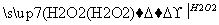 深黄色溶液
深黄色溶液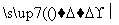 深黄色溶液
深黄色溶液
D.检验试液中的CO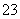 :试液
:试液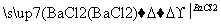 白色沉淀
白色沉淀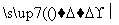 沉淀溶解
沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
两种短周期元素X和Y形成的单质能与氢气反应生成HX和HY,反应热分别为ΔH1和ΔH 2,已知ΔH1>ΔH 2,则判断一定正确的是
A.沸点:HY>HX B.还原性:HY>HX
C.稳定性:HY>HX D.酸性:HXO4>HYO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com