
【题目】已知:短周期元素A、B、C、D、E的原子序数依次增大。
①C的简单气态氢化物遇湿润的红色石蕊试纸变蓝色;
②A与D可以形成原子个数比分别为2∶1、1∶1的两种液态化合物X和Y,A、E同主族,C与B、D相邻;
③A、B、C、D四种元素组成一种化合物F,其组成原子数之比为5∶1∶1∶3。
请回答下列问题:
(1)C原子在周期表的位置为___________;写出化合物EDA的电子式________。
(2)C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐,写出其化学式________;
(3)F溶液与足量EDA的稀溶液混合加热,其离子方程式为_____________________。
(4)氯气与C的简单气态氢化物相遇有白烟及C2生成,写出反应方程式_____________。
(5)用CH4可以消除汽车尾气中氮氧化物的污染。
已知:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1
2NO2(g)![]() N2O4(g) ΔH=-56.9 kJ·mol-1
N2O4(g) ΔH=-56.9 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:___________________。
【答案】 第二周期第VA族 ![]() NH4NO3 HCO3—+NH4++2OH-
NH4NO3 HCO3—+NH4++2OH-![]() CO32-+2H2O+NH3↑ 8NH3+3Cl2
CO32-+2H2O+NH3↑ 8NH3+3Cl2![]() N2+6NH4Cl CH4(g)+N2O4(g)
N2+6NH4Cl CH4(g)+N2O4(g)![]() N2(g)+2H2O(l)+CO2(g) ΔH=-898.1 kJ·mol—1
N2(g)+2H2O(l)+CO2(g) ΔH=-898.1 kJ·mol—1
【解析】短周期元素A、B、C、D、E的原子序数依次增大。①C的简单气态氢化物遇湿润的红色石蕊试纸变蓝色,为氨气,则C为N元素;②A与D可以形成原子个数比分别为2∶1、1∶1的两种液态化合物X和Y,分别为水和过氧化氢,则A为H元素,D为O元素;A、E同主族,则E为Na元素,C与B、D相邻,则B为C元素;③A、B、C、D四种元素组成一种化合物F,其组成原子数之比为5∶1∶1∶3,F为NH4HCO3。
(1)C为N元素,在周期表中位于第二周期第VA族;化合物EDA为NaOH,属于离子化合物,电子式为![]() ;(2)硝酸与氨气化合生成NH4NO3;(3)F为NH4HCO3,与足量NaOH的稀溶液混合加热,离子方程式为HCO3-+NH4++2OH-
;(2)硝酸与氨气化合生成NH4NO3;(3)F为NH4HCO3,与足量NaOH的稀溶液混合加热,离子方程式为HCO3-+NH4++2OH-![]() CO32-+2H2O+NH3↑;(4)氯气与氨气相遇有白烟——氯化铵及N2生成,反应方程式为8NH3+3Cl2=N2+6NH4Cl;(5)已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1,②2NO2(g)=N2O4(g) ΔH=-56.9 kJ·mol-1,根据盖斯定律,将①-②得:CH4(g)+N2O4(g)=N2(g)+2H2O(l)+CO2(g) ΔH=(-955 kJ·mol-1)-(-56.9 kJ·mol-1)=-898.1 kJ·mol-1。
CO32-+2H2O+NH3↑;(4)氯气与氨气相遇有白烟——氯化铵及N2生成,反应方程式为8NH3+3Cl2=N2+6NH4Cl;(5)已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) ΔH=-955 kJ·mol-1,②2NO2(g)=N2O4(g) ΔH=-56.9 kJ·mol-1,根据盖斯定律,将①-②得:CH4(g)+N2O4(g)=N2(g)+2H2O(l)+CO2(g) ΔH=(-955 kJ·mol-1)-(-56.9 kJ·mol-1)=-898.1 kJ·mol-1。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是
A. 用铜电极电解NaCl溶液制备Cl2:2C1—+2H2O![]() Cl2↑+H2↑+2OH—
Cl2↑+H2↑+2OH—
B. 向MgCl2溶液中加入氨水制备Mg(OH)2:Mg2++2OH—==Mg(OH)2↓
C. 将FeS溶于稀硝酸制备Fe(NO3)3:FeS+4H++NO3==Fe3++NO↑+S↓+2H2O
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4—+6H++5H2O2==2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液。下列说法正确的是( )

A. a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O
B. 外电路电子的流向是从a到b
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. b电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g)![]() Fe(s)+CO2(g)△H>0.
Fe(s)+CO2(g)△H>0.
已知在1100°C时,该反应的化学平衡常数K=0.263.
①温度升高,平衡移动后达到新平衡,此时平衡常数值________(填“增大”“减小”“不变”);
②1100°C时测得高炉中,c(CO2)=0.025mol·L﹣1,c(CO)=0.1mol·L﹣1,则在这种情况下,该反应这一时刻向__________进行(填“左”或“右”).
(2)目前工业上也可用CO2来生产燃料甲醇CH3OH,有关反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),△H=﹣49.0KJmol﹣1,某温度下,向体积为1L恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
CH3OH(g)+H2O(g),△H=﹣49.0KJmol﹣1,某温度下,向体积为1L恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.

①反应开始至平衡,氢气的平均反应速率v(H2)=__________,CO2的转化率为_______.
该温度下上述反应的平衡常数K=____________(分数表示).
②反应达到平衡后,下列能使![]() 的值增大的措施是_________(填符号)。
的值增大的措施是_________(填符号)。
a.升高温度 b.再充入H2 c.再充入CO2
d.将H2O(g)从体系中分离 e.充入He(g)
③以8g甲醇为燃料,足量O2为氧化剂,250ml 浓度为1mol/L的KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极).写出燃料电池负极的电极反应式:_________________。
④有人提出,可以设计反应2CO(g)=2C(s)+O2(g)(△H>0)来消除CO的污染。请你判断上述反应是否能自发进行并说明理由__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(含有Cr2O3,FeO、Al2O3、SiO2等成分)为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O),其主要工艺流程如下:
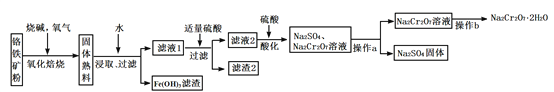
提示:熟料中含有Na2CrO4、NaFeO2等成分。
回答下列问题:
(1)将铬铁矿粉碎的目的是_____________________________ 。
(2)氧化焙烧时,生成Na2CrO4的化学方程式是__________。
(3)滤渣2中除Al(OH)3外还有__________(填化学式)。
(4)加入硫酸酸化的目的是__________________________。
(5)根据下图,请将操作a补充完整:________________,洗涤,干燥。
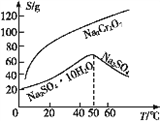
(6)控制105~110℃,向较浓的Na2Cr2O7溶液中加入KCl固体发生复分解反应,立即析出K2Cr2O7晶体。能生成K2Cr2O7晶体的原因是_____________。
(7)向Na2Cr2O7酸性溶液中加入过量FeSO4溶液,生成Cr3+和 Fe3+,再加入过量的强碱溶液生成铁铬氧体沉淀(CrxFe3-xO4)。加入过量强碱生成铁铬氧体沉淀的离子方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100mol·L-1NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和醋酸,滴定曲线如图。不考虑反应的热效应,下列说法正确的是

A. 曲线Ⅰ表示的是滴定盐酸的曲线
B. 滴定醋酸过程中,溶液中 增大
增大
C. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物E(结构简式为 )是合成消毒剂α——萜品醇(结构简式为
)是合成消毒剂α——萜品醇(结构简式为 )的中间体。由甲苯经一系列变化制取E的流程如下:
)的中间体。由甲苯经一系列变化制取E的流程如下:

请回答下列问题:
(1)化合物E中含有的官能团名称为________,α—萜品醇的分子式为_________,甲苯的结构简式为_____。
(2)反应I的化学方程式为____________。
(3)反应II的反应类型是__________________。
(4)反应III的试剂与条件为__________________。
(5)写出一种符合下列条件的有机物的结构简式_____________。
①是化合物D的一种同分异构体;②能与NaHCO3反应;③能与新制氢氧化铜浊液在加热条件下反应生成红色固体;④在核磁共振氢谱上有5个峰。
(6)下面是由化合物E合成一种α—萜品醇的流程的一部分,请将其中有G生成H的几步流程补充完整(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).________________。

提示:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明末宋应星的著书《天工开物》中记载了我国古代炼锌的方法,用炉甘石(主要成分是ZnCO3)和木炭混合加热分两步反应得到锌,写出其中氧化还原反应的化学方程式_____________。
现代工业上利用锌焙砂提炼金属锌的流程如下图所示(已知:①锌焙砂的主要成分是ZnO、ZnFe2O4,还含有少量FeO、CuO、NiO杂质;②金属活动性顺序:Zn>Ni>Cu),请回答下列问题:

(2)化合物ZnFe2O4中Fe的化合价为_________,酸浸时,ZnFe2O4发生反应的化学方程式为________。
(3)净化I操作分两步:首先用H2O2处理酸浸液,然后用物质A调节溶液的PH使Fe3+转化为Fe(OH)3沉淀过滤后除去。
①写出用H2O2处理酸浸液时发生反应的离子方程式______________。
②下图中的斜线是溶液中金属阳离子浓度(纵标)随pH值(横标)变化时的沉淀溶解平衡线,若加入物质A只使Fe3+沉淀完全,则物质A可能是_____________(填出一种可能的化学式),调节后溶液的pH应控制在______________范围内(假设杂质离子浓度均不大于0.1mol· L-1 )。
③此流程中没有用调节pH来除去Cu2+的原因是_____________。

(4)净化II欲分离出Cu、Ni,加入的B物质的化学式_____________。
(5)本流程中可以循环利用的化合物有_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“直接煤燃料电池”能够将煤中的化学能高效、清洁地转化为电能。用熔融Na2CO3作电解质的直接煤燃料电池的工作原理如图。下列有关说法正确的是

A. 该电池的总反应为C+O2=CO2
B. 煤直接燃烧发电比直接煤燃料电池发电的能量利用率高
C. 进入反应室的煤块粉碎成粉末状对反应速率和限度均无影响
D. 电子由电极b沿导线流向电极a,入口A加入的物质为煤粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com