
用下图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。
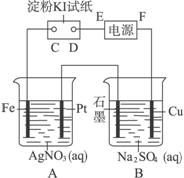
(1)A中发生反应的化学方程式为_________________________________。
(2)在B中观察到的现象是______________________________________。
(3)室温下,若从电解开始到时间t s,A、B装置中共收集到气体0.168 L(标准状况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1 000 mL,则A溶液的pH为__________________。
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源:2015-2016学年吉林省高一上学期12月月考化学试卷(解析版) 题型:填空题
(1)CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别之(简要地写出实验过程)
① 只允许用一种试剂________________
② 不用任何试剂________________
(2)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学情调查化学试卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A.用干燥的pH试纸测定新制氯水的pH
B.中和滴定实验中,洗净后的锥形瓶不需要干燥
C.用Na2S溶液与AlCl3溶液混合制取Al2S3
D.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期末理综化学试卷(解析版) 题型:填空题
工业生产硝酸铵的流程如下图所示:

(1)硝酸铵的水溶液呈 (填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为 。
(2)已知N2(g)+3H2(g) 2NH3(g) △H < 0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。
2NH3(g) △H < 0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。

①曲线a对应的温度是 。
②关于工业合成氨的反应,下列叙述正确的是 。
A.及时分离出NH3可以提高H2的平衡转化率
B.P点原料气的平衡转化率接近100%,是当前工业生产工艺中采用的温度、压强条件
C.上图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
D.M点比N点的反应速率快
E.如果N点时c(NH3)=0.2 mol·L-1,N点的化学平衡常数K ≈ 0.93 L2/mol2
(3)尿素[ CO(NH2)2 ]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272 kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138 kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式: 。
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下左图所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
②在上右图中画出第二步反应的平衡常数K随温度的变化的示意图。
(5)电解尿素[ CO(NH2)2 ]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期12月月考化学试卷(解析版) 题型:选择题
一定量的乙醇在氧气不足的情况下燃烧得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量为( )
A.1.4 g B.2.2 g
C.4.4 g D.在2.2~4.4 g之间
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:
Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
如果利用该电池精炼铜,则粗铜应连接的极是
A.NiOOH B.Ni(OH)2 C.Cd D.Cd(OH)2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列对有机物结构或性质的描述,错误的是( )
A.苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键
B. 将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应
C.乙烷和丙烯的物质的量共1mol,完全燃烧生成3molH2O
D.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高二上12月月考化学试卷(解析版) 题型:选择题
从人类生存的环 境考虑,未来理想的燃料应是
境考虑,未来理想的燃料应是
A.煤 B.氢气 C.石油炼制品 D.酒精
查看答案和解析>>
科目:高中化学 来源:2016届福建省闽粤联合体高三上学期第三次联考化学试卷(解析版) 题型:填空题
(1)下列有关说法正确的是
A.可用石灰水区分Na2CO3与NaHCO3溶液;
B.HClO4的酸性强于H2SO3,所以非金属性:Cl﹥S;
C.配制0.2 mol·L-1的Na2CO3溶液480mL,需称量10.6g Na2CO3固体;
D.金属钠着火时,可用泡沫灭火器来灭火;
E.强酸可以制弱酸,弱酸通过化学反应一定不能生成强酸;
F.过量的Zn和浓硫酸反应,生成标准状况下气体22.4L,转移电子一定是2mol;
G.SO2使品红溶液褪色和使KMnO4溶液褪色都体现了其漂白性。
(2)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、NO3-、Cl-、SO42-中的4种离子,所含离子均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。回答下列问题:
①溶液中存在的离子是 ;
②写出溶液中加入过量的稀硫酸反应的离子方程式____________________;
③向原溶液中滴加足量NaOH溶液后,过滤洗涤灼烧,最终得到固体质量为 g。
(3)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ、0.1 mol/L H3PO3溶液的pH = 1.7;
Ⅱ、H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ、H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是 。
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
写出H3PO3与过量NaOH溶液反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com