
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molH2、2molN2 | 4molH2、4molN2 | 2molNH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| N2的体积分数 | w 1 | w 2 | w 3 |
| 混合气体的密度(g•L-1) | ?ρ1 | ?ρ2 | ?ρ3? |
分析 (1)由 可知:
可知:
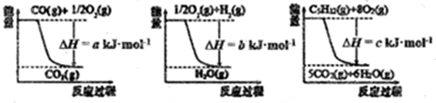
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-aKJ•mol;
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-bKJ•mol;
③C5H12(g)+8O2(g)=5CO2(g)+6H2O(g)△H=-cKJ•mol,由盖斯定律可知C5H12(g)+5H2O(g) $\frac{\underline{催化剂}}{△}$5CO(g)+11H2(g)△H=5①+11②-③;
(2)①化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变,结合反应的特点进行分析;
②3H2(g)+N2(g) $\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3(g)
初起(mol•L-1):2 2 0
变化(mol•L-1):1.5 0.5 1
平衡(mol•L-1):0.5 1.5 1
根据v=$\frac{△c}{△t}$计算,平衡常数等于平衡时生成物浓度幂之积比上反应物浓度幂之积;
③a.丙相当在甲的基础上减少氢气,平衡逆向移动,氮气的浓度增大,所以cl>c3;
b.乙相当在甲基础上增大压强,平衡正向移动,所以wl>w2;
c.根据ρ=$\frac{m}{V}$,体积相同,气体的质量越大密度越大,m乙>m甲>m丙,所以ρ2>ρ1>ρ3;
④将产物混合气中的氨冷却分离后,剩余气体循环使用,也可以使平衡正向移动,提高反应物的利用率;
(3)①容器甲中从正反应开始到达平衡,容器乙中从逆反应开始到达,平衡建立的途径不相同;
②温度相同时,甲乙两容器中达到的平衡相同,平衡常数相同,但绝热容器乙中所到达的平衡状态,相当于在容器甲中平衡的基础上降低温度,平衡向正反应移动;
③容器乙中所到达的平衡状态,相当于在容器甲中平衡的基础上降低温度,平衡向正反应移动.
解答 解:(1)由 可知:
可知:
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-aKJ•mol;
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-bKJ•mol;
③C5H12(g)+8O2(g)=5CO2(g)+6H2O(g)△H=-cKJ•mol,由盖斯定律可知C5H12(g)+5H2O(g) $\frac{\underline{催化剂}}{△}$5CO(g)+11H2(g)△H=5①+11②-③=c-5a-11b,
故答案为:c-5a-11b;
(2)①a.容器内混合气体的密度一直保持不变,不能作平衡的标志,故选;
b.3v正(N2)=v正(H2)═v逆(H2),达平衡状态,故不选;
c.容器内混合气体的平均相对分子质量保持不变,说明气体的物质的量不变,反应达平衡状态,故不选;
故答案为:a;
②3H2(g)+N2(g) $\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3(g)
初起(mol•L-1):2 2 0
变化(mol•L-1):1.5 0.5 1
平衡(mol•L-1):0.5 1.5 1
根据v(NH3)=$\frac{1mol/L}{20min}$=0.05mol•L-1•min-1,
K=$\frac{{1}^{2}}{0.{5}^{3}×1.5}$=5.33,
故答案为:0.05;5.33;
③a.丙相当在甲的基础上减少氢气,平衡逆向移动,氮气的浓度增大,所以cl>c3,故正确;
b.乙相当在甲基础上增大压强,平衡正向移动,所以wl>w2,故错误;
c.根据ρ=$\frac{m}{V}$,体积相同,气体的质量越大密度越大,m乙>m甲>m丙,所以ρ2>ρ1>ρ3,故正确;
故答案为:ac;
④将产物混合气中的氨冷却分离后,剩余气体循环使用,也可以使平衡正向移动,提高反应物的利用率,
故答案为:将产物混合气中的氨冷却分离后,剩余气体循环使用;
(3)①容器甲中从正反应开始到达平衡,容器乙中从逆反应开始到达,平衡建立的途径不相同,反应速率,甲正反应速率大于乙,故答案为:快;
B.温度相同时,甲乙两容器中达到的平衡相同,平衡常数相同,但绝热容器乙中所到达的平衡状态,相当于在容器甲中平衡的基础上降低温度,平衡向正反应移动,K(甲)<K(乙),故答案为:小;
C.容器乙中所到达的平衡状态,相当于在容器甲中平衡的基础上降低温度,平衡向正反应移动,故容器甲中的气体颜色比容器乙中的气体颜色深,故答案为:深.
点评 本题考查学生盖斯定律的应用、化学平衡移动及平衡常数与计算、合成氨条件的选择等,题目难度中等,关键是三行式的应用,要求学生要有扎实的基础知识和灵活应用知识解决问题的能力.


科目:高中化学 来源: 题型:解答题
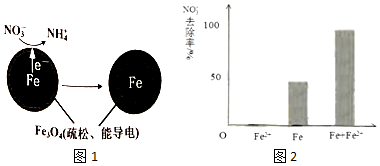
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
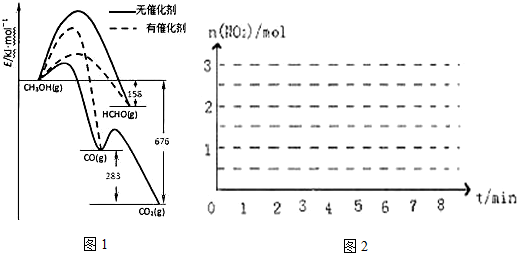
| 物质的量/mol 时间 | n(N2H4) | N(NO2) | N(N2) |
| 起始 | 2.0 | 3.0 | 0 |
| 第2min | 1.5 | a | 0.75 |
| 第4min | 1.2 | b | 1.2 |
| 第6min | 1.0 | c | 1.5 |
| 第7min | 1.0 | c | 1.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
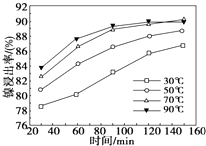 镍及其化合物具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.回答下列问题:
镍及其化合物具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合金的性质与其成分金属的性质不完全相同 | |
| B. | 工业上金属Mg、Al都是用电解熔融的氯化物制得的 | |
| C. | 黑色的氧化铜灼烧会变成砖红色 | |
| D. | 将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 诜项 | 实验操作 | 实验目的 |
| A | 将乙烯通入酸性KMnO4溶液中 | 证明乙烯能发生加成反应 |
| B | 向含酚酞的NaOH溶液中加入氯水 | 证明Cl2具有漂白性 |
| C | 常温下,向Fe和Cu中分别加入浓硝酸 | 比较Fe和Cu的金属活动性 |
| D | 将铁钉放入试管中,下端浸入食盐水中 | 验证铁的吸氧腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com