
 +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl3+2H2O
+3FeCl3+2H2O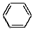 +3H2$→_{△}^{催化剂}$
+3H2$→_{△}^{催化剂}$
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
科目:高中化学 来源: 题型:选择题
| A. | 任何物质燃烧都必须有氧气参加 | |
| B. | 氢气在氯气中燃烧发出淡蓝色火焰,并在空气中产生大量白雾 | |
| C. | 饱和氯水在光照下有气泡产生,该气体为氯气 | |
| D. | 长久放置的氯水将失去漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何晶体中,若含有阳离子也一定含有阴离子 | |
| B. | 原子晶体中只含有共价键 | |
| C. | 离子晶体中只含有离子键 | |
| D. | 分子晶体中只存在分子间作用力,不含化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
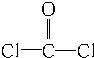 和双酚A:
和双酚A: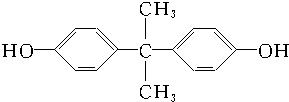 缩聚而成,其反应方程式为
缩聚而成,其反应方程式为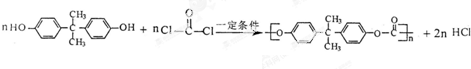 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在洁净的试管中加入1-2 mL AgNO3溶液,再加入过量浓氨水,振荡,混合均匀 | |
| B. | 在洁净的试管中加入1-2 mL浓氨水,再加入AgNO3溶液至过量 | |
| C. | 在洁净的试管中加入1-2 mL稀氨水,再逐滴加入2%AgNO3溶液至过量 | |
| D. | 在洁净的试管中加入2%AgNO3溶液1-2 mL,逐滴加入2%稀氨水至沉淀恰好溶解为止 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12N4 | B. | C4H8N4 | C. | C6H10N4 | D. | C6H8N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
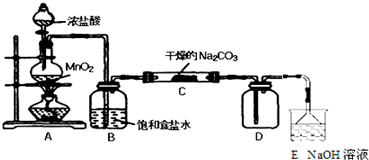
| 实 验 步 骤 | 预 期 现 象 和 结 论 |
| 步骤1:取C中的少量固体样品于试管中, 加入蒸馏水至固体溶解,然后各取1~2mL 所得溶液分别置于甲、乙两支试管中. | 得到无色溶液. |
| 步骤2:向甲试管中加入过量的BaCl2溶液, 静置. | 若溶液变浑浊,证明固体中含有Na2CO3. |
| 步骤3:取甲试管中上层清液少许于另一只 试管中,滴加少量澄清石灰水, 充分振荡. | 若上层清液变浑浊, 证明固体中含有NaHCO3. |
| 步骤4:向乙试管中先加入过量的稀HNO3 稀HNO3;再滴入少量AgNO3溶液溶液. | 若生成白色沉淀;证明固体中含有氯化钠. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
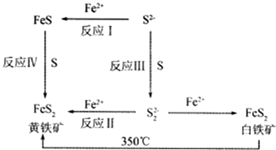 Ⅰ.Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为2Li++FeS+2e-═Li2S+Fe,则该电池的总反应式为2Li+FeS═Li2S+Fe.
Ⅰ.Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为2Li++FeS+2e-═Li2S+Fe,则该电池的总反应式为2Li+FeS═Li2S+Fe.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com