
����Ŀ���ش����и�С���е����⣨NA��6.02![]() 1023mol-1�����㣩
1023mol-1�����㣩
��1��1.806��1023��KClO3��K+��ClO3-�����ʵ���֮��Ϊ______��
��2��0.1molNa2SO4��Լ����_________��Na+��
��3����34gNH3������ͬԭ������H2O�����ʵ���Ϊ��_______________��
��4��32gCH4���________mol������
��5��1.806��1023��H2SO4�к���ԭ�ӵ����ʵ���Ϊ________mol��
��6��1����ԭ������Ϊag����1mol O������Ϊ______g��
��7��2gH2��1molSO2ԭ����Ŀ֮�ȣ�_______________��
��8���ڱ�״���£���1.7gNH3������ͬԭ������CO�����Ϊ��_______________��
��9���ڱ�״���£���1.12LCH4������ͬԭ������H2O���ӵĸ���Ϊ��_______________��
���𰸡� 1:1 1.204![]() 1023 2.67mol 20 1.2 6.02
1023 2.67mol 20 1.2 6.02![]() 1023a 1:2 4.482 5.02
1023a 1:2 4.482 5.02![]() 1022
1022
��������������������⿼�����ʵ��������������ʵ���������״������������֮���ת����ϵ���Լ�������ɵķ�����
��1��KClO3��K+��ClO3-�����ʵ���֮��Ϊ1:1��
��2��0.1molNa2SO4�к���Na+���ʵ���Ϊ0.2mol��Na+����Ϊ0.2![]() 6.02
6.02![]() 1023=1.204
1023=1.204![]() 1023��
1023��
��3��n��NH3��=34g![]() 17g/mol=2mol������ԭ�����ʵ���Ϊ8mol����8molԭ��H2O�����ʵ���Ϊ8mol
17g/mol=2mol������ԭ�����ʵ���Ϊ8mol����8molԭ��H2O�����ʵ���Ϊ8mol![]() 3=2.67mol��
3=2.67mol��
��4��n��CH4��=32g![]() 16g/mol=2mol��1��CH4�к���10�����ӣ�32gCH4�к��е��������ʵ���Ϊ20mol��
16g/mol=2mol��1��CH4�к���10�����ӣ�32gCH4�к��е��������ʵ���Ϊ20mol��
��5��n��H2SO4��=1.806![]() 1023
1023![]() ��6.02
��6.02![]() 1023mol-1��=0.3mol������ԭ�����ʵ���Ϊ0.3mol
1023mol-1��=0.3mol������ԭ�����ʵ���Ϊ0.3mol![]() 4=1.2mol��
4=1.2mol��
��6��1molO�к�6.02![]() 1023����ԭ�ӣ�1����ԭ������Ϊag��1mol O������Ϊ6.02
1023����ԭ�ӣ�1����ԭ������Ϊag��1mol O������Ϊ6.02![]() 1023ag��
1023ag��
��7��n��H2��=2g![]() 2g/mol=1mol�����к��е�n��H��=2mol��1molSO2�к��е�ԭ�����ʵ���Ϊ3mol��2gH2��1molSO2ԭ����Ŀ֮��Ϊ2:3��
2g/mol=1mol�����к��е�n��H��=2mol��1molSO2�к��е�ԭ�����ʵ���Ϊ3mol��2gH2��1molSO2ԭ����Ŀ֮��Ϊ2:3��
��8��n��NH3��=1.7g![]() 17g/mol=0.1mol�����к��е�ԭ�����ʵ���Ϊ0.4mol����0.4molԭ�ӵ�CO�����ʵ���Ϊ0.2mol���ڱ�״���µ����Ϊ0.2mol
17g/mol=0.1mol�����к��е�ԭ�����ʵ���Ϊ0.4mol����0.4molԭ�ӵ�CO�����ʵ���Ϊ0.2mol���ڱ�״���µ����Ϊ0.2mol![]() 22.4L/mol=4.48L��
22.4L/mol=4.48L��
��9��n��CH4��=1.12L![]() 22.4L/mol=0.05mol����������ԭ�����ʵ���Ϊ0.25mol����0.25molԭ�ӵ�H2O�����ʵ���Ϊ0.25mol
22.4L/mol=0.05mol����������ԭ�����ʵ���Ϊ0.25mol����0.25molԭ�ӵ�H2O�����ʵ���Ϊ0.25mol![]() =
=![]() mol������H2O���ӵĸ���Ϊ
mol������H2O���ӵĸ���Ϊ![]() mol
mol![]() 6.02
6.02![]() 1023mol-1=5.02
1023mol-1=5.02![]() 1022��
1022��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
��������ˮ��pHΪ7.0�������pHС��7.0��
���ϸ�ִ�л�����β���ŷű������ڷ�ֹ������Ⱦ��
��Fe2O3��������ɫ�����Ϳ�ϣ�
��ʹ������������ˮ���������У����ɵ��л��Ȼ�����ܶ������к���
��SiO2��������̫���ܵ�ء�
A. �٢ڢ� B. �٢ܢ�
C. �ڢۢ� D. �ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȥ���������л�����������ʣ�����������Ϊ���ʣ����ܴﵽĿ�ĵ���
A. ��������(����)�����뱥��̼������Һ��������ú�Һ
B. ��(����)������Ũ��ˮ������
C. �Ҵ�(ˮ)����������ƣ�����
D. ����(��ϩ)��ͨ�����Ը��������Һ��ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����pH=2��HX��Һ��HY��Һ��1mL ���ֱ��ˮϡ�ͣ���ҺpH����Һ����仯��������ͼ��ʾ������˵����ȷ����
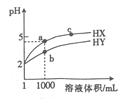
A. a��c�����ӦHX�ĵ���ƽ�ⳣ����K(c)>K(a)
B. a��b�����Ӧ����Һ�У�c(X-)>c(Y-��
C. �����ʵ���Ũ�ȵ�NaX��NaY�Ļ����Һ�У�c(HY)>c(HX)
D. �ֱ���10mL0.1mol/LHX��Һ��10mL 0.1mol/L HY��Һ�еμ�ͬŨ�ȵ�����������Һ��pH = 7����������������Һ���ٵ���HX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���������������ء�����˵����ȷ���ǣ� ��
A.������DZͧ��Я���������Ƶ�Ŀ����ɱ�����������Ϻ�����ȫ����
B.������пǿ���������к��д���пԪ��
C.��ȼú�м���CaO���ƹ��͵����������綯������������ɫ��ѧ����
D.����ұ�����������ʵ����ɶ������ȷ�Ӧ��������ʴ���������ʵ����Ķ��Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��Ⱥ����Ӽ��ֺ����ۼ����ǣ� ��
A. Na2O B. NH3 C. Ca(OH)2 D. CaBr2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ������������x��y��z�������Ȱ��ֶ�����Ԫ��ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯����ͼ��ʾ��

����˵����ȷ����
A. xԪ�������ڱ��е�λ���ǵڶ����ڢ�A��
B. ���Ӱ뾶��g2->h->d2->e+>f3+
C. ����������Ӧˮ��������ԣ�y>z
D. ��̬�⻯������ȶ��ԣ�g>h
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����6.5 g Zn����500mLϡ�����У�Zn��HCl��ǡ����ȫ��Ӧ�����㣺
��1��6.5 g Zn�����ʵ���_______________��
��2�����ɵ������ڱ�״���µ����_____________��
��3��ԭϡ��������ʵ���Ũ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ò���©��������ƿ�ӳ�ˮ�ù��˳�������ȷ�IJ�����
A.�ȹ�ˮ��ͷ�����³���ƿ�ϵ���Ƥ�ܣ���ȡ�²���©��
B.��ȡ�²���©�����ٹ���ˮ��ͷ
C.�Ƚ���������ֽһ��ȡ�����ٹ���ˮ��ͷ
D.�Ȱ��³���ƿ�ϵ���Ƥ�ܣ�����ˮ��ͷ����ȡ�²���©��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com