
| A. | Cl-的结构示意图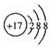 | |
| B. | S2-的结构示意图: | |
| C. | 纯碱的化学式:NaHCO3 | |
| D. | 硫酸的电离方程式:H2SO4═H2++SO42- |
分析 A.氯离子的核电荷数为17,核外电子总数为18,最外层满足8电子稳定结构;
B.硫离子的最外层含有8个电子;
C.纯碱为碳酸钠的俗名,碳酸氢钠为小苏打;
D.硫酸电离出的氢离子不能合并.
解答 解:A.Cl-的核外电子总数为18,其离子结构示意图为 ,故A正确;
,故A正确;
B. 为硫原子的原子结构示意图,硫离子最外层达到8电子稳定结构,其正确的离子结构示意图为:
为硫原子的原子结构示意图,硫离子最外层达到8电子稳定结构,其正确的离子结构示意图为: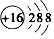 ,故B错误;
,故B错误;
C.NaHCO3为碳酸氢钠,俗名为小苏打,纯碱为碳酸钠,正确的化学式为:Na2CO3,故C错误;
D.硫酸为强电解质,在溶液中完全电离,其正确的电离方程式为:H2SO4═2H++SO42-,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及原子结构示意图、离子结构示意图、化学式、电离方程式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:实验题

| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水和酒精 |
| B | 17.9 | 290 | 1.26 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、HBr、HI、HF的沸点依次升高 | |
| B. | 氨分子中N-H键的极性小于水分子中O-H键的极性 | |
| C. | 乙醇分子间存在氢键,乙醛分子间不存在氢键,故乙醇的沸点高于乙醛 | |
| D. | 由于N-H键强于P-H键,故NH3的沸点高于PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12倍 | B. | 24倍 | C. | 48倍 | D. | 96倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无法比较 | B. | Q1<Q2 | C. | Q1=Q2 | D. | Q1>Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 碘酒 | 分散系 | 混合物 |
| B | 液氯 | 电解质 | 化合物 |
| C | 硫酸钠 | 盐 | 纯净物 |
| D | NaHSO4 | 酸式盐 | 电解质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com