
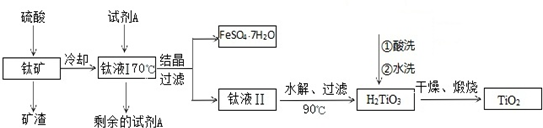
分析 (1)由酸溶、水解方程式可知均为未发生氧化还原反应,酸溶中生成FeSO4,可知FeTiO3中铁的化合价;
(2)(3)加入硫酸后FeTiO3、Fe2O3溶解,SiO2不反应,过滤除去SiO2,由于亚铁离子易被氧化,钛液I加入试剂A,将溶液中Fe3+还原为Fe2+,超过90℃TiOSO4(aq)水解得到H2TiO3(s),冷却至70℃左右结晶出硫酸亚铁晶体,过滤分离出硫酸亚铁晶体,钛液Ⅱ水解析出H2TiO3(s),洗涤、干燥、灼烧得到TiO2;
(4)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是亚铁离子,直接水洗时Fe2+会水解得到氢氧化亚铁,氧化得到氢氧化铁,灼烧氢氧化铁分解得到氧化铁.
解答 解:加入硫酸后FeTiO3、Fe2O3溶解,SiO2不反应,过滤除去SiO2,由于亚铁离子易被氧化,钛液I加入试剂A,将溶液中Fe3+还原为Fe2+,超过90℃TiOSO4(aq)水解得到H2TiO3(s),冷却至70℃左右结晶出硫酸亚铁晶体,过滤分离出硫酸亚铁晶体,钛液Ⅱ水解析出H2TiO3(s),洗涤、干燥、灼烧得到TiO2;
(1)由酸溶、水解方程式可知均为未发生氧化还原反应,酸溶中生成FeSO4,可知FeTiO3中铁的化合价为+2价,
故答案为:+2;
(2)因为矿石经硫酸溶解后得到的Fe2(SO4)3,而后面过滤得到的是FeSO4•7H2O,所以试剂A是铁粉,
故答案为:铁粉;
(3)由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3,经过滤进入FeSO4•7H2O中,导致产品TiO2产率降低,
故答案为:由于TiOSO4容易水解,若温度过高,则会有较多的TiOSO4水解为固体H2TiO3,而经过滤进入FeSO4•7H2O中,导致TiO2产率降低;
(4)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是Fe2+离子,直接水洗时Fe2+会水解得到氢氧化亚铁,氧化得到氢氧化铁,灼烧氢氧化铁分解得到氧化铁,煅烧后获得的TiO2发黄的杂质是Fe2O3,
故答案为:Fe2+;Fe2O3.
点评 本题属于化学工艺流程题目,涉及对操作与试剂的分析评价、对原理的分析评价、物质的分离提纯等,需要学生熟练掌握元素化合物知识,培养了学生实验能力、知识迁移应用能力,难度中等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | 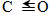 | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 876 | 465 | 413 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Cl2与足量的NaOH溶液反应,转移的电子数为2NA | |
| B. | 0.1molZn与含0.1molHCl的盐酸充分反应,转移的电子数目为0.2NA | |
| C. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA | |
| D. | 向FeI2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移的电子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
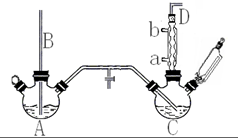 氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
氯苯是重要的有机化工产品,是染料、医药、有机合成的中间体,工业上常用“间歇法”制取.反应原理、实验装置图(加热装置都已略去)如下:
| 项目 | 二氯苯 | 尾气 | 不确定苯耗 | 流失总量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向Na2SiO3溶液中通入少量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 铝粉投入NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| D. | AlCl3溶液中加入足量氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将湿衣服放在太阳下晒干 | B. | 向较多粉尘的地面洒水后再清洁 | ||
| C. | 铁制栏杆喷涂油漆 | D. | 将食盐密封好,防止吸潮结块 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com