
 X��Y��Z��W����Ԫ�����ڱ��е�ǰ������Ԫ�أ����ǵĺ˵������������Xԭ�ӵ������p����ĵ���Ϊ������ṹ��Y�ǵؿ��к�������Ԫ�أ�ZԪ���γɵ�һ�ֻ����ﳣ������ˮ����WԪ���ǵ�������Ԫ����δ�ɶԵ���������Ԫ�أ�WCl3����X��Y���⻯���γ�����λ��������������������ʵ���֮��Ϊ2��1��1mol�������������AgNO3��Һ��Ӧ������3molAgCl����ش��������⣺
X��Y��Z��W����Ԫ�����ڱ��е�ǰ������Ԫ�أ����ǵĺ˵������������Xԭ�ӵ������p����ĵ���Ϊ������ṹ��Y�ǵؿ��к�������Ԫ�أ�ZԪ���γɵ�һ�ֻ����ﳣ������ˮ����WԪ���ǵ�������Ԫ����δ�ɶԵ���������Ԫ�أ�WCl3����X��Y���⻯���γ�����λ��������������������ʵ���֮��Ϊ2��1��1mol�������������AgNO3��Һ��Ӧ������3molAgCl����ش��������⣺���� X��Y��Z��W����Ԫ�����ڱ��е�ǰ������Ԫ�أ����ǵĺ˵������������Y�ǵؿ��к�������Ԫ�أ���YΪOԪ�أ�Xԭ�ӵ������p����ĵ���Ϊ������ṹ�����������Ų�Ϊ2s22p3����XΪNԪ�أ�ZԪ���γɵ�һ�ֻ����ﳣ������ˮ������ZΪAl��WԪ���ǵ�������Ԫ����δ�ɶԵ���������Ԫ�أ���Χ�����Ų�Ϊ3d54s1����WΪCr��CrCl3����NH3��H2O����λ��������������������ʵ���֮��Ϊ2��1��1mol�������������AgNO3��Һ��Ӧ������3molAgCl����������ȫ����磬��������[Cr��NH3��4��H2O��2]Cl3���ݴ˽��
��� �⣺X��Y��Z��W����Ԫ�����ڱ��е�ǰ������Ԫ�أ����ǵĺ˵������������Y�ǵؿ��к�������Ԫ�أ���YΪOԪ�أ�Xԭ�ӵ������p����ĵ���Ϊ������ṹ�����������Ų�Ϊ2s22p3����XΪNԪ�أ�ZԪ���γɵ�һ�ֻ����ﳣ������ˮ������ZΪAl��WԪ���ǵ�������Ԫ����δ�ɶԵ���������Ԫ�أ���Χ�����Ų�Ϊ3d54s1����WΪCr��CrCl3����NH3��H2O����λ��������������������ʵ���֮��Ϊ2��1��1mol�������������AgNO3��Һ��Ӧ������3molAgCl����������ȫ����磬��������[Cr��NH3��4��H2O��2]Cl3��
��1��NH3���������ܼ�������Һ����ԭ���ǣ��������Ӽ����γɷ��Ӽ������ͬ������ԭ����������һ�����ܳ��������ƣ�Y��OԪ�أ��������ڣ��ڶ����ڣ��е�һ��������������Ԫ����FԪ�أ�
�ʴ�Ϊ���������Ӽ����γɷ��Ӽ������F��
��2��NO3-������Nԭ�Ӽ۲���Ӷ���Ϊ3+$\frac{5+1-2��3}{2}$=3��û�йµ��Ӷԣ������幹����ƽ�������Σ�������Nԭ�Ӳ�ȡsp2�ӻ���
�ʴ�Ϊ��ƽ�������Σ�sp2��
��3��Cr3+�ĺ�������Ų�ʽ��1s22s22p63s23p63d3��WCl3�γɵ�����λ������ﻯѧʽΪ��[Cr��NH3��4��H2O��2]Cl3��
�ʴ�Ϊ��1s22s22p63s23p63d3��[Cr��NH3��4��H2O��2]Cl3��
��4��������Alԭ����ĿΪ4��Feԭ����ĿΪ1+8��$\frac{1}{8}$+6��$\frac{1}{2}$+12��$\frac{1}{4}$=8���ʸúϽ�Ļ�ѧʽΪFe2Al����������Ϊ$\frac{4��27+56��8}{{N}_{A}}$g���������ı߳�Ϊa nm����Ͻ���ܶ�Ϊ$\frac{4��27+56��8}{{N}_{A}}$g�£�a��10-7cm��3=$\frac{5.56��1{0}^{23}}{{a}^{3}{N}_{A}}$g•cm-3��
�ʴ�Ϊ��Fe2Al��$\frac{5.56��1{0}^{23}}{{a}^{3}{N}_{A}}$��
���� �����Ƕ����ʽṹ�Ŀ��飬�漰��������Ų��������ܡ�������ӻ����ۡ����ӹ��͡�������������ȣ�ע������������ڽ�����������ʲ�ͬ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����ʵ | ���� |
| A | ����������ͨ����ˮ�У���ˮ��ɫ | ����������Ư���� |
| B | ����84������Һ����NaClO������Ʒ����Һ�У���ɫ��������ͬʱ����ʳ�ף���ɫ�ܿ���Ϊ��ɫ | ����ҺpH��С����84������Һ����������ǿ |
| C | ͭ����ϡ�����У������������ټ��������ƹ��壬��Һ���������������ݷų���ͭ�ܽ� | �����ƿ��Լӿ�ͭ��ϡ���ᷴӦ���� |
| D | ������ϡ���Ṳ�ȣ��ټ�������Һˮԡ���ȣ����������� | ����û��ˮ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
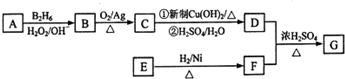
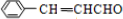 ��
��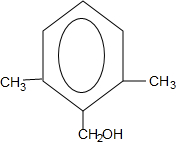 ��
��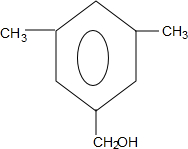 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ͼ�ļ���ʽ��ʾ��������Ϊ��3-��-4-�һ�-7-������ | |
| B�� | ���Ϸ���ʽΪC3H8O�Ĵ������ֲ�ͬ�Ľṹ | |
| C�� | ��ϩ��һ���������ܷ����ӳɷ�Ӧ���Ӿ۷�Ӧ�����ữ���������Һ������Ҳ����һ�������±��������������� | |
| D�� |  ����ű���������أ���ͼ��������ʽ��C15H20O5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
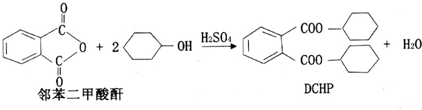
| A�� | DCHP�ķ���ʽΪC20H28O4 | |
| B�� | �����Ʊ�DCHP�ķ�Ӧ����ȡ����Ӧ | |
| C�� | DCHP�����ϵ�һ�ȴ�����4�� | |
| D�� | 1 mol DCHP�����뺬4 mol NaOH����Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵��������ǣ�������
�����⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵��������ǣ�������| A�� | ��طŵ�ʱNa+��a��������b���� | |
| B�� | �缫b����MnO2��MnO2�����缫�������л�ԭ���� | |
| C�� | �õ�صĸ�����ӦΪ��BH4-+8OH--8e-=BO2-+6H2O | |
| D�� | ÿ����3 mol H2O2��ת�Ƶĵ���Ϊ6 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�0.05 mol•L-1 Fe2��SO4��3��Һ�к�Fe3+��ĿΪ0.1NA | |
| B�� | ��״���£�22.4 L�ױ��к�C-H��ĿΪ8NA | |
| C�� | ���³�ѹ�£�3.2 g O2��O3������У���ԭ�ӵ���ĿΪ0.2NA | |
| D�� | 0.1 mol Na2O2������CO2��Ӧʱ��ת�Ƶĵ�����ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com