
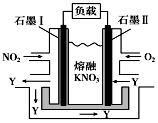
 某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )| A. | 该电池放电时K+向石墨Ⅰ电极迁移 | |
| B. | 石墨Ⅰ附近发生的反应:NO2-e-+NO3-═N2O5 | |
| C. | O2在石墨Ⅱ附近发生氧化反应,Y为NO | |
| D. | 相同条件下,放电过程中消耗的NO2和O2的体积比为2:1 |
分析 以NO2、O2、熔融KNO3组成的燃料电池,在使用过程中石墨I电极为原电池的负极,NO2被氧化,N元素化合价升高,应生成N2O5,电极方程式为NO2+NO3--e-═N2O5,石墨Ⅱ通入氧气,发生还原反应,为原电池的正极,电极方程式为O2+2N2O5+4e-═4NO3-,以此解答该题.
解答 解:A.石墨Ⅱ通入氧气,发生还原反应,为原电池的正极,原电池中阳离子移向正极,则K+向石墨Ⅱ电极迁移,故A错误;
B.石墨I为原电池的负极,发生氧化反应,电极方程式为NO2+NO3--e-═N2O5,故B正确;
C.石墨Ⅱ通入氧气,发生还原反应,负极的NO2被氧化,N元素化合价升高,Y应是N2O5,故C错误;
D.电极方程式分别为4NO2+4NO3--4e-═4N2O5、O2+2N2O5+4e-═4NO3-,则放电过程中消耗的NO2和O2的体积比为4:1,故D错误;
故选B.
点评 本题考查了燃料电池,为高频考点,侧重于学生的分析能力的考查,注意正负极的判断、由化合价的变化推测电极产物等,侧重于有关原理的应用的考查,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2的化合物.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个Na+的NaOH溶于1L水中形成溶液的物质的量浓度为lmol•L-1 | |
| B. | 总质量为18g的H216O和H218O所含分子数为NA | |
| C. | 常温常压下,22.4L的CO2与Mg完全反应,转移电子数为4NA | |
| D. | 硫酸的摩尔质量与NA个硫酸分子的质量在数值上相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 结论 | |
| A | 将SO2通人溴水中 | 溴水颜色褪去 | SO2具有漂白性 |
| B | 将铁屑放入稀HNO3中 | 放出无色气体 | Fe比H2活泼 |
| C | 将澄清石灰水滴入某溶液 | 生成白色沉淀 | 溶液中存CO32- |
| D | 将乙烯通入KMnO4酸性溶液 | KMnO4颜色褪去 | 乙烯具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
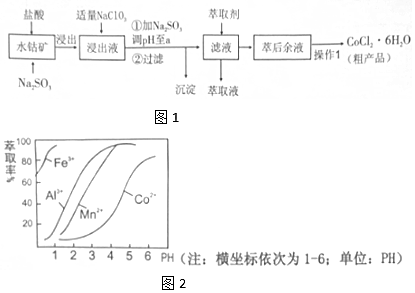
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氟化氢的电子式: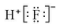 | |
| B. | 氯原子的结构示意图: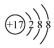 | |
| C. | 丙烯的结构简式:C3H6 | |
| D. | 硫原子的最外层电子排布式:3s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(ClO-)=c(OH-) | B. | c(ClO-)+c(OH-)═c(Na+) | ||
| C. | c(OH-)═c(HClO)+c(H+) | D. | 2c(ClO-)+2c(HClO)═c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜跟硝酸反应:CuO+2H+═Cu2++H2O | |
| B. | NO2气体与水反应:2NO2+H2O═2H++NO3-+NO↑ | |
| C. | 硫酸和氢氧化钡溶液反应:SO42-+H++OH-+Ba2+═BaSO4↓+H2O | |
| D. | AlCl3溶液中加入氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com