
MOH和ROH两种一元碱的溶液分别加水稀释10n倍时,pH变化与n的关系如图所示。下列叙述中正确的是
( )
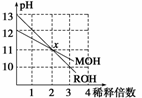
A.MOH和ROH都是强碱
B.稀释前,[ROH]=10[MOH]
C.常温下pH之和为14的醋酸和ROH溶液等体积混合,所得溶液呈碱性
D.在x点,[M+]=[R+]
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
“分类”的思想方法,在化学发展中起到了重要作用.下列分类标准合理的是 ( )
A. 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
B.只含一种元素的物质一定是单质
C.溶于水后能电离出H+的化合物都为酸
D.有单质生成的反应一定是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
我国某大城市今年夏季多次降下酸雨.据环保部门测定,该城市整个夏季酸雨的pH平均为3.2.在这种环境中的铁制品极易被腐蚀.对此条件下铁的腐蚀的叙述不正确的是( )
|
| A. | 此腐蚀过程有化学腐蚀也有电化学腐蚀 |
|
| B. | 发生电化学腐蚀时的正极反应为 2H2O+O2+4e﹣═4OH﹣ |
|
| C. | 在化学腐蚀过程中有氢气产生 |
|
| D. | 发生电化学腐蚀时的负极反应为Fe﹣2e﹣═Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在给定条件下能大量共存的是( )
A.在pH=1的溶液中:NH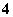 、K+、ClO-、Cl-
、K+、ClO-、Cl-
B.有SO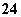 存在的溶液中:Na+、Mg2+、Ca2+、I-
存在的溶液中:Na+、Mg2+、Ca2+、I-
C.有NO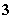 存在的强酸性溶液中:NH
存在的强酸性溶液中:NH 、Ba2+、Fe2+、Br-
、Ba2+、Fe2+、Br-
D.在[H+]=1.0×10-13 mol·L-1的溶液中:Na+、S2-、[Al(OH)4]-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某溶液中由水电离的[H+]=1×10-13 mol·L-1,该溶液可能是( )
①三氧化硫水溶液 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中[Na+]>[A-],则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中[HA]________[A-];
(2)混合溶液中[HA]+[A-]________0.1 mol·L-1;
(3)混合溶液中由水电离出的[OH-]______0.2 mol·L-1 HA溶液中由水电离出的[H+];
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________NaA的水解程度。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁粉可与高温水蒸气反应,若反应后得到的干燥固体质量比反应前铁粉的质量增加了32 g,则参加反应的铁粉的物质的量是( )
A.0.5 mol B.1 mol
C.1.5 mol D.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,实线表示放热反应X(g)+Y(g)Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按虚线进行,可采取的措施是( )
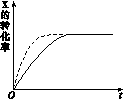
A.升高温度 B.加大X的投入量
C.加催化剂 D.增大体积
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.铝盐(明矾溶液)和铁盐(硫酸铁溶液)都有净水作用,两者的作用原理是相同的
B.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
C.0.1mol/L的CH3COONa溶液的pH约为9,说明CH3COOH是弱酸
D.室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中导电粒子的数目减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com