
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ·mol-1) | 786 | 715 | 3401 |
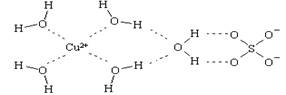
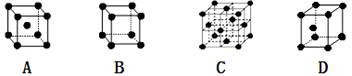
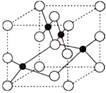
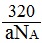
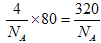 ,因此体积是
,因此体积是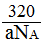 cm3。
cm3。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.1∶1 | B.1∶2 |
| C.1∶3 | D.2∶3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子晶体中一定存在分子间作用力,不一定存在共价键 |
| B.H2O比H2S稳定,是因为H2O分子间能形成氢键而H2S不能 |
| C.晶体中含阳离子就一定含阴离子 |
| D.基态24Cr原子的电子排布式为:〔Ar〕3d44s2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
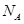 表示阿伏加德罗常数,则立方氮化硼晶胞体积为 cm3。
表示阿伏加德罗常数,则立方氮化硼晶胞体积为 cm3。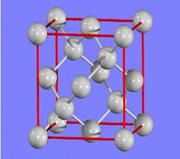
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.正丁烷与异丁烷 |
| B.红磷与白磷 |
| C.H2和D2 |
| D.石英与干冰 E. 金刚石与水晶 F. 氧气和臭氧 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.冰融化时,分子中H—O键发生断裂 |
| B.分子晶体中,分子间作用力越大,通常熔点越高 |
| C.分子晶体中,共价键键能越大,分子的熔、沸点越高 |
| D.分子晶体中,分子间作用力越大,分子越稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com