
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)=c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH${\;}_{4}^{+}$)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O${\;}_{4}^{2-}$)+c(HC2O${\;}_{4}^{-}$)+c(OH-)=c(Na+)+c(H+) |
分析 A.反应后溶质为等浓度的醋酸和氯化钠,醋酸在溶液中部分电离,溶液显示酸性,则c(CH3COO-)>>c(OH-);
B.一水合氨的电离程度大于铵根离子的水解程度,c(NH4+)>c(NH3•H2O),再根据物料守恒分析;
C.根据混合液中的物料守恒分析;
D.根据混合液中的电荷守恒判断.
解答 解:A.0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合,反应生成等浓度的醋酸和NaCl,钠离子和氯离子不水解,醋酸在溶液中部分电离出氢离子,则c(CH3COO-)>>c(OH-),溶液中正确的离子浓度大小为:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-),故A错误;
B.0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合,一水合氨的电离程度大于铵根离子的水解程度,c(NH4+)>c(NH3•H2O),根据物料守恒可知:c(NH4+)>c(Cl-)>c(NH3•H2O),故B错误;
C.0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合,根据物料守恒可得:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),即:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),故C正确;
D.0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合,根据电荷守恒可知:2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+),故D正确;
故选CD.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为巨大的关键,注意掌握电荷守恒、物料守恒及盐的水解原理的含义,试题培养了学生的分析、理解能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Cl02气体是一种常用的消毒剂,我国从2000年起逐步用Cl02代替氯气对饮用水进行消毒.但二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热.
Cl02气体是一种常用的消毒剂,我国从2000年起逐步用Cl02代替氯气对饮用水进行消毒.但二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2悬浊液 | 金属钠 | |
| A | 中和反应 | - | 溶解 | 产生氢气 |
| B | - | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| C | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | - |
| D | 水解反应 | - | - | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只要在室内放一盆水 | |
| B. | 向地势低的地方撤离 | |
| C. | 观察风向,顺风撤离 | |
| D. | 用湿毛巾或蘸有弱碱性溶液的毛巾捂住口鼻撤离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
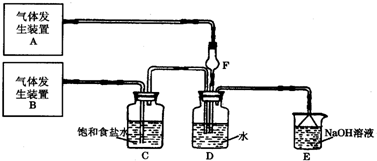
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Na+、Cl- | B. | Fe3+、Na+、Cl-、SO42- | ||
| C. | NH4+、Na+、NO3-、CO32- | D. | Na+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com