
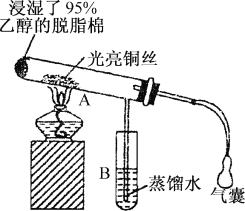
����Ŀ���йش����Ĵ�����������ɴ����Ҵ�������ʵ�����õ�һЩ��ʶ����ʵ��װ����ͼ��ʾ��ʵ�����Ϊ��Ԥ��ʹ���Ž��Ҵ���������ͼװ�úã���ͭ˿���м䲿�ּ��ȣ�Ƭ�̺�ʼ�н��ࣨ��Ъ�ԣ��ع�����������ɹ۲쵽���Ե�ʵ������
��ش��������⣺
��1�������ȵ�ͭ˿��������Ӧ�Ļ�ѧ����ʽΪ��________��
��2����A���пɹ۲쵽_______��ʵ�������п���ʶ���ڸ�ʵ������У������������ʱ�μ��˻�ѧ��Ӧ��������ʶ�������������ʱ��Ҫһ����_______��
��3����֪����������Ӧ�Ƿ��ȷ�Ӧ����ʵ�����һ��ʱ������ֻ�����ƾ��ƣ���Ӧ���ܷ�������У�______��ԭ���ȵ�ͭ˿����ʲô����_______��
��4����֤�Ҵ���������Ļ�ѧ������_______��
���𰸡�2CH3CH2OH��O2![]() 2CH3CHO��2H2O ���Ȳ��ֵ�ͭ˿���Ъ�Եع��������������ֱ���ٱ�� �¶� ��Ӧ�Կɼ������� �Կɿ���ԭ���Ȳ��ֵ�ͭ˿������ֱ�ڱ������� ʵ�������ж��װ��B��ʢ������ˮ���Թܣ�����ȡ��������Һ��������Ӧ��ʵ��[��������Cu(OH)2����Һ���ȵ�ʵ��]������֤���Ҵ���ͭ�Ĵ�����������ȩ�Ľ���
2CH3CHO��2H2O ���Ȳ��ֵ�ͭ˿���Ъ�Եع��������������ֱ���ٱ�� �¶� ��Ӧ�Կɼ������� �Կɿ���ԭ���Ȳ��ֵ�ͭ˿������ֱ�ڱ������� ʵ�������ж��װ��B��ʢ������ˮ���Թܣ�����ȡ��������Һ��������Ӧ��ʵ��[��������Cu(OH)2����Һ���ȵ�ʵ��]������֤���Ҵ���ͭ�Ĵ�����������ȩ�Ľ���
��������
(1)�����ȵ�ͭ˿�����Ҵ�������������ȩ��ˮ��
(2)����ʱ��Cu����������CuO��Ȼ��CuO�����Ҵ�������ȩ��Cu��ˮ��
(3)���ݴ���������Ӧ�Ƿ��ȷ�Ӧ�����жϣ�
(4)�Ҵ�������Ϊ��ȩ������ȩ���ļ��鷽������ʵ����ơ�
(1)�����ȵ�ͭ˿�����Ҵ�������������ȩ��ˮ����Ӧ�Ļ�ѧ����ʽΪ2CH3CH2OH+O2![]() 2CH3CHO+2H2O���ʴ�Ϊ��2CH3CH2OH+O2
2CH3CHO+2H2O���ʴ�Ϊ��2CH3CH2OH+O2![]() 2CH3CHO+2H2O��
2CH3CHO+2H2O��
(2)����ʱ��Cu����������CuO��2Cu+O2![]() 2CuO��Ȼ��CuO�����Ҵ�������ȩ��Cu��ˮ���ظ�����������Ӧ����ɹ۲쵽A�����Ȳ��ֵ�ͭ˿���Ъ�Եع��������������ֱ�ڱ�������п���ʶ���ڸ�ʵ������У������������ʱ�μ��˻�ѧ��Ӧ��������ʶ�������������ʱ��Ҫһ�����¶ȣ��ʴ�Ϊ�����Ȳ��ֵ�ͭ˿���Ъ�Եع��������������ֱ�ڱ�죻�¶ȣ�
2CuO��Ȼ��CuO�����Ҵ�������ȩ��Cu��ˮ���ظ�����������Ӧ����ɹ۲쵽A�����Ȳ��ֵ�ͭ˿���Ъ�Եع��������������ֱ�ڱ�������п���ʶ���ڸ�ʵ������У������������ʱ�μ��˻�ѧ��Ӧ��������ʶ�������������ʱ��Ҫһ�����¶ȣ��ʴ�Ϊ�����Ȳ��ֵ�ͭ˿���Ъ�Եع��������������ֱ�ڱ�죻�¶ȣ�
(3)����������Ӧ�Ƿ��ȷ�Ӧ����Ӧ�ų��������ܹ�ά�ַ�Ӧ�������У���˳����ƾ��ƣ���Ӧ�Խ��У�ԭ���Ȳ��ֵ�ͭ˿�Կɿ���������ֱ�ڱ������ʴ�Ϊ����Ӧ�Կɼ������У��Կɿ���ԭ���Ȳ��ֵ�ͭ˿������ֱ�ڱ�������
(4)�Ҵ�������Ϊ��ȩ����ȩ����ȩ�������л�ԭ�ԣ��ܱ�������Һ������������ͭ����Һ��������֤��ȩ����IJ���Ϊ��ʵ�������ж��װ��B��ʢ����������ˮ���Թ��У��������Ƶ�������Һˮԡ���ȣ��۲��Թܱ����Ƿ��й������������ɣ���ȡB�е�Һ�����Թ��У��������Ƶ�������ͭ����Һ���ȣ��۲��Ƿ��к�ɫ�ij������ɣ��ʴ�Ϊ��ʵ�������ж��װ��B��ʢ������ˮ���Թܣ�����ȡ��������Һ��������Ӧ��ʵ��[��������Cu(OH)2����Һ���ȵ�ʵ��]������֤���Ҵ���ͭ�Ĵ�����������ȩ�Ľ��ۡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
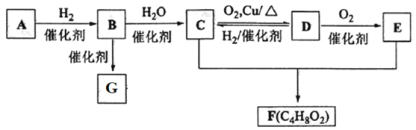
����Ŀ����֪��̬��A�ڱ�״���µ��ܶ���1.16 g��L1��B�IJ���������������һ������ʯ�ͻ�����չˮƽ��G��һ�ָ߷��ӻ�������� A��B��C��D��E��F��G �������¹�ϵ��
��ش�
(1)D�еĹ�����������_______________�� B�ĽṹʽΪ_________��
(2)д�� C+E��F��Ӧ�Ļ�ѧ����ʽ__________��
(3)д�� C��D��Ӧ�Ļ�ѧ����ʽΪ__________��
(4)��֪������ A ��һ�������¿ɺϳɲ���ʹ���� KMnO4 ��Һ��ɫ���л��д���úϳɷ�Ӧ�Ļ�ѧ����ʽ___________����Ӧ����Ϊ___________��
(5)�����й�������ȷ����_____________��
a. A��B��C��D��E��F��G��Ϊ�ǵ����
b. A������ԭ�Ӳ����ܴ���ͬһƽ����
c. ����ʱ��D ��������������ͭ����Һ��Ӧ����ש��ɫ����
d.75%(�������)�� C ˮ��Һ������ҽ������
e. ���̶���С���ƿ�Ͷ�� C �У��ƿ鸡��Һ���ϣ����д������ݲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤�����ԣ�Cl2 > Fe3+ >SO2��ij��ѧ�о���ѧϰС����ͼ��ʾװ�ý���ʵ�飨�г�������A�еļ���װ�����ԣ��������Ѿ�������ϣ���
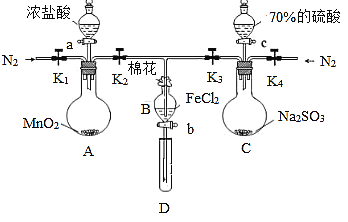
��.���ɼ�K1��K4��ͨ��һ��ʱ��N2���ٽ�T�͵��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1,K3,K4��
��.����a���μ�һ������Ũ���ᣬ��A���ȡ�
��.��B����Һ���ʱ��ֹͣ���ȣ��н����ɼ�K2��
��.����b��ʹԼ2mL����Һ����D�Թ��У��������е������ӡ�
��.���ɼ�K3������c������70%�����ᣬһ��ʱ���н����ɼ�K3��
��.�����Թ�D���ظ����̢�������B��Һ�е����ӡ�
�ش��������⣺
��1�����̢��Ŀ����________��
��2�����н������ҺΪ________��������_____________��
��3�����²��������Һ��Ƶ����ӷ�Ӧ��____����_____����д�Լ���ѧʽ�������������������____��
��4����˵��������Fe3��>SO2�����ӷ���ʽ��________��
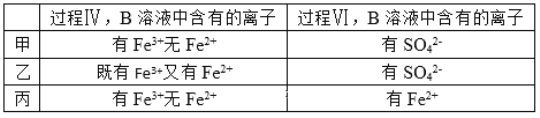
��5���ס��ҡ�����λͬѧ�ֱ����������ʵ�飬���ǵļ����һ���ܹ�֤�������ԣ�Cl2> Fe3��>SO2����__����ס����ҡ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ӱ�����ǵ�����ͽ�������˲�ȡ������Դ�ṹ���������ŵȴ�ʩ������PM2.5��SO2��NOx����Ⱦ����ش���������:
��. ������������������������������ķ�Ӧ֮һΪ��2NO2(g)+O3(g)![]() N2O5(g)+O2(g)����ͬ�¶��£����������������з����÷�Ӧ�������Ϣ���±���ͼ��ʾ���ش��������⣺
N2O5(g)+O2(g)����ͬ�¶��£����������������з����÷�Ӧ�������Ϣ���±���ͼ��ʾ���ش��������⣺
���� | �� | �� |
�ݻ�/L | 1 | 1 |
�¶�/K | T1 | T2 |
��ʼ������ | 1molO3��2molNO2 | 1molO3��2molNO2 |
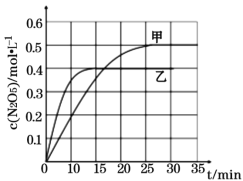
��0~15min���������з�Ӧ��ƽ�����ʣ�v(NO2) =____(������������λС��)��
�ڸ÷�Ӧ������ӦΪ____(����ȡ����ȡ�)��Ӧ��
��T1ʱƽ���������������ٳ���1molO3��2molNO2���ٴ�ƽ���NO2�İٷֺ�����____(�������С�����䡱)��
�ܷ�Ӧ��ϵ���¶�ΪT1ʱ��ƽ�ⳣ��Ϊ____��
���ں��º��������£�������������֤���÷�Ӧ�Ѿ��ﵽƽ�����____��
a�������ڻ������ѹǿ���ٸı�
b������2n molNO2��ͬʱ��������n molO3
c����������ƽ����Է����������ٸı�
d����������ܶȲ��ٸı�
II. ij��ѧС��������Ϻ��֪��2NO(g)��O2(g) ![]() 2NO2(g) �ķ�Ӧ���̷�������
2NO2(g) �ķ�Ӧ���̷�������
��2NO(g)��N2O2(g) (��)�� v1����k1����c2(NO)��v1����k1����c(N2O2)��
��N2O2(g)��O2(g)��2NO2(g) (��) v2����k2����c(N2O2)��c(O2)��v2����k2����c2(NO2)��
��ش��������⣺
��1����֪����2NO(g)��O2(g) ![]() 2NO2(g)��Ӧ���ʵ��Ƿ�Ӧ�ڣ���Ӧ�ٵĻ��E1�뷴Ӧ�ڵĻ��E2�Ĵ�С��ϵΪE1____E2(���������������)��
2NO2(g)��Ӧ���ʵ��Ƿ�Ӧ�ڣ���Ӧ�ٵĻ��E1�뷴Ӧ�ڵĻ��E2�Ĵ�С��ϵΪE1____E2(���������������)��
��2��һ���¶��£���Ӧ2NO(g)��O2(g) ![]() 2NO2(g)�ﵽƽ��״̬��д����k1����k1����k2����k2����ʾƽ�ⳣ���ı���ʽK��____��
2NO2(g)�ﵽƽ��״̬��д����k1����k1����k2����k2����ʾƽ�ⳣ���ı���ʽK��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У����ڷ�Ӧ��������Ũ�Ȳ���ı䷴Ӧ�������(����)
A.CO2ͨ�����ʯ��ˮ��B.̼��������ȼ��
C.����������ӦD.��˿��������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���ý����ƻ�ԭCCl4��SiCl4�Ƶ�һ��һάSiC���װ�����ط�Ӧ�Ļ�ѧ����ʽΪ8Na+CCl4+SiCl4![]() SiC+8NaCl������˵������ȷ����
SiC+8NaCl������˵������ȷ����
A. һάSiC���װ����ȱ��������С�����н�ǿ����������
B. ������Ӧ��SiC���������������ǻ�ԭ����
C. SiCl4���ɼ��Լ����ɵķǼ��Է���
D. ÿ����1 mol SiCת��8 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����(���� )
A. ��״���£�22.4L���Ȼ�̼������ΪNA
B. �����£�16gO2��O3��ɵĻ�������������е�ԭ����ΪNA
C. ������,1mol/L��AlCl3��Һ�к��е�Cl-������Ϊ3NA
D. 18gNH4+�����������ĵ�������Ϊ12NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������к���KAl(SO4)2���������ֽ����������һ�������¿�ʵ����ͼ��ʾ���ʼ�ת����
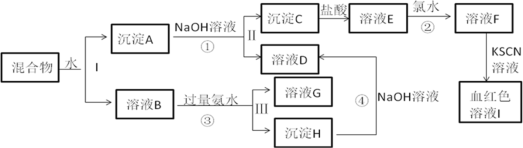
��֪��Cl2+2Fe2+==2Fe3++2Cl-
��ش��������⣺
(1)����H�Ļ�ѧʽ_________����ͼ��Ѫ��ɫ������______(�ѧʽ)
(2)��������������IJ����������ձ������������Ҫ___________��
(3)��Ӧ�ٵ����ӷ���ʽ��____________��
(4)������ҺG�н��������ӵIJ���������������___________��
(5)����E�м���KSCN��Һ����Һ����ɫ�������C��________(������)��
����E�м���KSCN��Һ����Һ���ɫ��Ϊ��һ��ȷ�ϳ���C�ijɷ֣��������¶���ʵ��: ������C��5mol/L����14mLǡ����ȫ�ܽ⣬������Һ�������ձ�״����56mL������ʹ����Fe2+ȫ��ת��ΪFe3+�������C���ܵĻ�ѧʽ��__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮMgBr2������������ʵ���Ҳ���þм��Һ��Ϊԭ���Ʊ���ˮMgBr2��װ����ͼ1����Ҫ�������£�
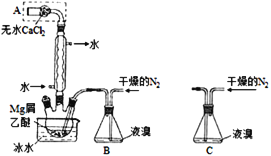
ͼ1 ͼ2
����1������ƿ��װ��10gþм��150mL��ˮ���ѣ�װ��B�м���15mLҺ�壻
����2������ͨ�����ĵ�����ֱ������ȫ��������ƿ�У�
����3����Ӧ��Ϻ�ָ������£����ˣ���Һת������һ�������ƿ�У���ȴ��0�棬�������壬�ٹ��˵������Ѻ��廯þ��Ʒ��
����4���������ñ��ܽ��Ʒ����ȴ��0�棬�������壬���ˣ�ϴ�ӵ������Ѻ��廯þ��������160��ֽ����ˮMgBr2��Ʒ��
��֪����Mg��Br2��Ӧ���ҷ��ȣ�MgBr2����ǿ��ˮ�ԣ�
��MgBr2+3C2H5OC2H5![]() MgBr23C2H5OC2H5
MgBr23C2H5OC2H5
��ش�
(1)����A��������______��
(2)ʵ���в����ø�������������N2��ԭ����______________��
(3)����3�У���һ�ι��˳�ȥ��������_________________��
(4)�йز���4��˵������ȷ����__________________��
A������95%���Ҵ����汽�ܽ��Ʒ B��ϴ�Ӿ����ѡ��0��ı�
C��������160�����ҪĿ���dz�ȥ�� D���ò����Ŀ���dz�ȥ���ѺͿ��ܲ�������
(5)Ϊ�ⶨ��Ʒ�Ĵ��ȣ�����EDTA(��дΪY)����Һ�ζ�����Ӧ�����ӷ���ʽ��Mg2++Y4���TMgY2
�ٵζ���ϴ��ǰ�IJ�����_______________________��
�ڲⶨʱ���ȳ�ȡ0.2500g��ˮMgBr2��Ʒ���ܽ����0.0500molL��1��EDTA����Һ�ζ����յ㣬����EDTA����Һ25.00mL��������ˮMgBr2��Ʒ�Ĵ�����__________(������������ʾ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com