
| A、室温下,10L,pH=13的NaOH溶液中含有Na+的数目为NA |
| B、常温常压下,17g氨气中含有氢原子的数目为NA |
| C、1mol/L的Na2SO3溶液1L加热蒸干得到固体产物转移的电子数目为4NA |
| D、体积为1L、物质的量浓度为1mol?L-1的Na2CO3溶液中含有NA个CO32- |
| 17g |
| 17g/mol |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
 )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )| A、可以与NaHCO3溶液反应产生CO2 |
| B、可以与乙醇发生酯化反应 |
| C、可以发生银镜反应 |
D、苹果酸与 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图所示,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图所示,下列关于该分子说法正确的是( )| A、该化合物分子式为 C15H20O4 |
| B、该物质可以发生加成反应和氧化反应,但不能发生取代反应和消去反应 |
| C、2mol该物质与足量溴水反应消耗单质溴480g |
| D、该化合物在一定条件下可与FeCl3溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、①②④ |
| C、①②③ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业酒精中含有乙醇和甲醇 |
| B、煤中含有苯和甲苯 |
| C、天然油脂中含有高级脂肪酸甘油酯 |
| D、许多水果中含有酯类化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应显示硫酸具有酸性 |
| B、NH4CuSO3中硫元素被氧化 |
| C、刺激性气味的气体是二氧化硫 |
| D、反应中硫酸作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、冰熔化时,分子中H-O键发生断裂 |
| B、NaOH中只含有离子键 |
| C、CO2与SiO2都属于分子晶体 |
| D、熔沸点由高到低的顺序是金刚石>NaCl>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P: 100kPa |
5 | 5.6 | 6.4 | 6.8 | 7 | 7 |
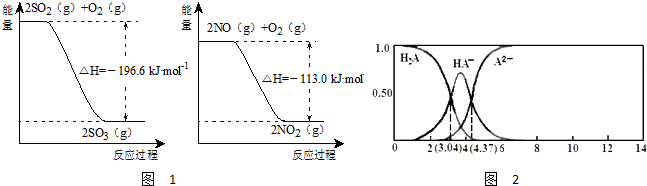
| c(A2-) |
| c(HA-) |
| c(H+) |
| c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com