
【题目】化学与生产、生活密切相关。下列叙述正确的是( )
A.煤的干馏和煤的液化均是物理变化
B.天然纤维和合成纤维的主要成分都是纤维素
C.海水淡化的方法有蒸馏法、电渗析法等
D.用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同
科目:高中化学 来源: 题型:
【题目】
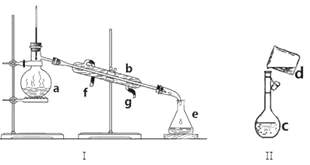
(1)写出下列仪器的名称:
a. b. c. e.
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。冷凝水由 (填f或g)口通入。
(3)现需配制0.1mol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。
②根据计算得知,用托盘天平所需称量NaOH的质量为 g。
③配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)________。
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶 |
B.称量计算出的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解并冷却至室温 |
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中 |
D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)物质的量浓度误差分析:(填偏高、偏低、无影响)
①用滤纸称量氢氧化钠 ;
②定容时,若眼睛俯视刻度线,则所配制的溶液浓度将 ;
③未冷却到室温就注入容量瓶定容 ;
④配好的溶液转入干净的试剂瓶时,不慎溅出部分溶液 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、H、N三种化学元素在组成人体的化学成分中,质量分数共占73%左右,而在组成岩石圈的化学成分中,质量分数还不到1%,这一事实说明了( )
A. 生物界与非生物界具有相似性
B. 生物界与非生物界具有统一性
C. 生物界与非生物界具有差异性
D. 生物界与非生物界的元素组成是不同的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲、乙、丙三种不同物质(不含结晶水)的溶解度曲线图。下列有关叙述正确的是()
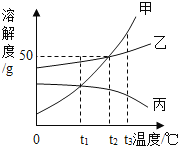
A. t1℃时,分别取出相同质量的甲、丙两种饱和溶液升温到t2℃时,甲和乙溶质的质量分数相等
B. t2℃时,将甲、乙两种饱和溶液分别恒温蒸发等质量的水,析出晶体的质量可能不等
C. 将三种饱和溶液分别从t3℃降低到t2℃时,甲和乙溶质的质量分数减小,丙的溶质的质量分数不变
D. 当甲的饱和溶液中含有少量乙时,可以采取冷却热饱和溶液的办法提取乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验需要0.80 mol·L-1NaOH溶液475 mL和0.40 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
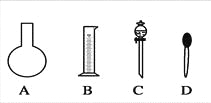
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)下列操作中,不能用容量瓶实现的有______________(填序号)。
A.配制一定体积准确浓度的标准溶液 |
B.量取一定体积的液体 |
C.测量容量瓶规格以下的任意体积的液体 |
D.准确稀释某一浓度的溶液 |
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为___________g。在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度_________(填”大于”、“等于”或“小于”,下同)0.8 mol·L-1。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度__________0.8 mol·L-1。
(4)根据计算得知,所需质量分数为98 %、密度为1.84 mol·L-1的浓硫酸的体积为__________mL(计算结果保留一位小数)。如果实验室有10 mL、15 mL、20 mL、50 mL量筒,选用___________mL量筒最好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒温恒容密闭容器中,发生反应:A(g)+B(g)![]() 2C(g) △H=-QkJ/mol,保持其它条件不变,只改变起始加入量,测得相关数据如表所示:
2C(g) △H=-QkJ/mol,保持其它条件不变,只改变起始加入量,测得相关数据如表所示:

下列说法中错误的是()
A. α1+α2=1;Φ2=Φ1 B.Φ3=2Φ1 ;Q3=2Q1
C.Φ3=Φ1=Φ2;Q3=2Q1 D. α1=α3;Q1+Q2=Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个温度和体积不变的容器中,硫可以发生如下变化,其反应过程和能量关系如图1所示。(SO2(g)+1/2O2(g)![]() SO3(g) △H=-98.45kJ·mol-1)
SO3(g) △H=-98.45kJ·mol-1)
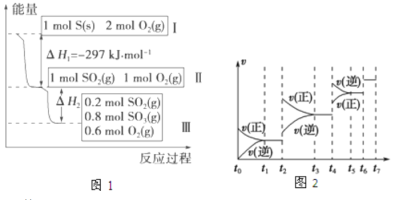
(1)硫燃烧的热化学方程式为 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有 。
A.降低温度 B.充入He C.再充入1mol SO2(g)和1mol O2(g) D.使用催化剂
(3)恒温恒容时,图1中II到III反应放出的热量比1mol SO2和2mol O2充分反应放出的热量 (填
“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 。(如t1~t2、t3~t4、t5~t6、t6~t7等)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则下列说法正确的是
A. 一个16O原子的质量为16 g
B. 17O的相对原子质量约为17
C. 氧元素的相对原子质量为![]()
D. 氧元素的相对原子质量为(16a%+17b%+18c%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com